CHAPITRE 17: Items 82 et 224 Occlusions veineuses rétiniennes
Dr A. Couturier, Hôpital Lariboisière, AP-HP, Paris
Situations cliniques de départ
Les occlusions veineuses rétiniennes peuvent être évoquées dans les situations cliniques suivantes.
 42 – Hypertension artérielle : savoir que c’est un des principaux facteurs de risque associé à la survenue des occlusions veineuses rétiniennes (OVR). Connaître l’existence de l’artériolosclérose rétinienne et le mécanisme du signe du croisement et pourquoi il peut aboutir à une occlusion de branche veineuse rétinienne.
42 – Hypertension artérielle : savoir que c’est un des principaux facteurs de risque associé à la survenue des occlusions veineuses rétiniennes (OVR). Connaître l’existence de l’artériolosclérose rétinienne et le mécanisme du signe du croisement et pourquoi il peut aboutir à une occlusion de branche veineuse rétinienne.
 138 – Anomalie de la vision : les OVR se manifestent par une baisse de l’acuité visuelle le plus souvent unilatérale, brutale, plus ou moins profonde (selon l’étendue et la localisation du territoire occlus et selon la forme ischémique ou non de l’occlusion), avec un œil blanc et indolore.
138 – Anomalie de la vision : les OVR se manifestent par une baisse de l’acuité visuelle le plus souvent unilatérale, brutale, plus ou moins profonde (selon l’étendue et la localisation du territoire occlus et selon la forme ischémique ou non de l’occlusion), avec un œil blanc et indolore.
 152 – œil rouge et/ou douloureux : savoir qu’un glaucome néovasculaire est une cause d’œil rouge et douloureux. Savoir qu’un glaucome néovasculaire peut être une complication d’une forme ischémique d’OVCR, qu’il nécessite une prise en charge en urgence et entraîne une perte de vision le plus souvent irréversible.
152 – œil rouge et/ou douloureux : savoir qu’un glaucome néovasculaire est une cause d’œil rouge et douloureux. Savoir qu’un glaucome néovasculaire peut être une complication d’une forme ischémique d’OVCR, qu’il nécessite une prise en charge en urgence et entraîne une perte de vision le plus souvent irréversible.
 178 – Demande/prescription raisonnée et choix d’un examen diagnostique : savoir que le bilan d’une OVR doit rester limité au bilan des facteurs de risques cardiovascu-laires en cas d’OVR chez un sujet âgé. Un bilan plus poussé des facteurs de la coagulation ne sera proposé qu’en cas d’OVCR chez un sujet de moins de 50 ans. Connaître les examens complémentaires utiles et sans risque pour le diagnostic et le suivi des OVR et de leurs complications : l’angiographie fluorescéinique pour le bilan de l’ischémie rétinienne, la tomographie par cohérence optique (OCT) pour le bilan de l’œdème maculaire.
178 – Demande/prescription raisonnée et choix d’un examen diagnostique : savoir que le bilan d’une OVR doit rester limité au bilan des facteurs de risques cardiovascu-laires en cas d’OVR chez un sujet âgé. Un bilan plus poussé des facteurs de la coagulation ne sera proposé qu’en cas d’OVCR chez un sujet de moins de 50 ans. Connaître les examens complémentaires utiles et sans risque pour le diagnostic et le suivi des OVR et de leurs complications : l’angiographie fluorescéinique pour le bilan de l’ischémie rétinienne, la tomographie par cohérence optique (OCT) pour le bilan de l’œdème maculaire.
 251 – Prescrire des corticoïdes par voie générale ou locale : savoir que les injections intravitréennes de corticoïdes peuvent être prescrites comme traitement d’un œdème maculaire secondaire à une OVR. Connaître les effets secondaires potentiels des corticoïdes intravitréens (cataracte, glaucome).
251 – Prescrire des corticoïdes par voie générale ou locale : savoir que les injections intravitréennes de corticoïdes peuvent être prescrites comme traitement d’un œdème maculaire secondaire à une OVR. Connaître les effets secondaires potentiels des corticoïdes intravitréens (cataracte, glaucome).
 352 – Expliquer un traitement au patient : expliquer que les injections intravitréennes peuvent être prescrites en cas d’œdème maculaire compliquant une OVR. Connaître 304quels produits et les stratégies de traitement peuvent être proposés pour traiter un œdème maculaire. Dans les formes ischémiques, savoir expliquer en quoi la photocoagulation laser est nécessaire pour éviter les complications liées à la néovascularisation rétinienne (mais qu’elle ne permet pas d’améliorer la vision).
352 – Expliquer un traitement au patient : expliquer que les injections intravitréennes peuvent être prescrites en cas d’œdème maculaire compliquant une OVR. Connaître 304quels produits et les stratégies de traitement peuvent être proposés pour traiter un œdème maculaire. Dans les formes ischémiques, savoir expliquer en quoi la photocoagulation laser est nécessaire pour éviter les complications liées à la néovascularisation rétinienne (mais qu’elle ne permet pas d’améliorer la vision).
Hiérarchisation des connaissances
| Rang | Rubrique | Intitulé et descriptif |
|
|
Identifier une urgence | Conduite à tenir devant une baisse de vision brutale avec œil blanc et identification des urgences |
|
|
Identifier une urgence | Reconnaître une urgence hypertensive et une HTA maligne Définition d’une crise hypertensive et d’une urgence hypertensive |
|
|
Identifier une urgence | Savoir évoquer un décollement de rétine : description sémiologique |
|
|
Prévalence, épidémiologie | Épidémiologie de l’HTA, HTA facteur de risque cardiovasculaire majeur : prévalence, liens (âge, obésité, diabète, etc.), complications cardiovasculaires, répartition HTA essentielle et secondaire |
|
|
Définition | Connaître la définition, la signification et la démarche étiologique devant une cécité monoculaire transitoire |
|
|
Définition | Définition de l’HTA Définitions HAS et SFHTA (seuils : consultation, MAPA, automesure, grades de sévérité) |
|
|
Définition | Connaître la définition de l’HTA chez l’enfant et l’existence de normes pédiatriques |
|
|
Définition | Connaître les facteurs de risque majeurs, indépendants, modifiables (tabac, HTA, diabète, dyslipidémie) et non modifiables (âge, sexe masculin, hérédité) |
|
|
Définition | Définition d’une HTA résistante Connaître les facteurs de résistance (non-observance, sel, syndrome d’apnée du sommeil, médicaments ou substances hypertensives, etc.) |
|
|
Diagnostic positif | Savoir déterminer si un trouble visuel est mono- ou binoculaire |
|
|
Diagnostic positif | Savoir interpréter un réflexe photomoteur direct et consensuel |
|
|
Diagnostic positif | Savoir évoquer le diagnostic d’aura migraineuse : AIT, crise épileptique partielle |
|
|
Diagnostic positif | Connaître les méthodes de mesure de la PA (consultation, automesure, MAPA) et interpréter |
|
|
Diagnostic positif | Connaître les signes d’orientation en faveur d’une HTA secondaire Savoir mener l’examen clinique et prescrire les examens complémentaires permettant d’évoquer une HTA secondaire |
|
|
Diagnostic positif | Évaluation initiale d’un patient hypertendu : circonstances de découverte, interrogatoire, risque cardiovasculaire, examen clinique |
|
|
Diagnostic positif | Mesure de la pression artérielle (PA) chez l’enfant Connaître les indications de mesure de la PA chez l’enfant (examen systématique annuel après 3 ans, en cas de facteur de risque) et en connaître les modalités (brassards adaptés, abaques pour l’âge et le sexe) |
|
|
Diagnostic positif | Connaître les signes cliniques des affections vasculaires de la rétine (OACR, OVCR), leurs complications (néovascularisation, glaucome néovasculaire, œdème maculaire) et les principes de traitement |
|
|
Diagnostic positif | Connaître les signes cliniques d’une neuropathie optique (NOIA, NORB, œdème papillaire) |
|
|
Diagnostic positif | Connaître les diagnostics différentiels de l’aura migraineuse : décollement de rétine, glaucome, hémorragie du vitré |
|
|
Diagnostic positif | Connaître la présentation clinique, les modes de survenue, les facteurs de risque des décollements de rétine |
|
|
Diagnostic positif | Connaître les signes cliniques d’une hémorragie du vitré et ses principales causes : acuité visuelle, champ visuel, PEV, OCT |
|
|
Diagnostic positif | Connaître la démarche diagnostique en cas de suspicion d’HTA secondaire : clinique, biologie, imagerie |
|
|
Étiologies | Connaître les principales causes d’atteinte des voies optiques et du nerf optique et identifier les étiologies nécessitant une prise en charge urgente (NOIAA, œdème papillaire) |
|
|
Étiologies | Connaître les principales causes d’HTA secondaire : néphropathies parenchymateuses, HTA rénovasculaire, causes endocriniennes, coarctation de l’aorte, etc. |
|
|
Étiologies | Connaître les principales causes d’HTA chez l’enfant |
|
|
Prise en charge | Connaître la stratégie du traitement médicamenteux de l’HTA : traitement initial, classes thérapeutiques, adaptation, surveillance, chiffres cibles de PA |
|
|
Prise en charge | Connaître les situations cliniques particulières pouvant orienter le choix du traitement antihypertenseur |
|
|
Prise en charge | Connaître les particularités du traitement antihypertenseur du sujet âgé de plus de 80 ans |
|
|
Prise en charge | Connaître les principaux effets indésirables et contre-indications des traitements antihypertenseurs |
|
|
Prise en charge | Prise en charge d’une urgence hypertensive |
|
|
Prise en charge | Principes de prise en charge d’une HTA secondaire : HTA rénovasculaire et endocrinienne |
|
|
Suivi et/ou pronostic | Complications de l’HTA, retentissement sur les organes cibles : neurosensorielles, cardiovasculaires, rénales |
|
|
Suivi et/ou pronostic | Plan de soins à long terme et modalités de suivi d’un patient hypertendu : savoir évaluer l’efficacité du traitement, la tolérance au traitement et l’observance du patient |
|
|
Examens complémentaires | Connaître les principaux examens complémentaires en ophtalmologie et leurs indications : atteinte du segment antérieur, du nerf optique, de la rétine (AV, angiographie, OCT maculaire, ERG) |
|
|
Examens complémentaires | Indications de l’imagerie devant un trouble visuel récent |
|
|
Contenu multimédia | Interpréter un réflexe photomoteur direct et consensuel |
|
|
Contenu multimédia | Photographie d’un œdème papillaire |
|
|
Contenu multimédia | Photographie d’un champ visuel des deux yeux avec hémianopsie (quadranopsie) latérale homonyme (ou bitemporale), y compris déficit pupillaire afférent relatif |

307![]() L’occlusion veineuse rétinienne (OVR) est une pathologie vasculaire de la rétine. Elle correspond à une obstruction du système de drainage veineux rétinien. Il s’agit d’une pathologie fréquente, en particulier chez le sujet âgé présentant des facteurs de risques vasculaires. Elle représente l’affection vasculaire rétinienne la plus fréquente après la rétinopathie diabétique et une cause importante de baisse de vision.
L’occlusion veineuse rétinienne (OVR) est une pathologie vasculaire de la rétine. Elle correspond à une obstruction du système de drainage veineux rétinien. Il s’agit d’une pathologie fréquente, en particulier chez le sujet âgé présentant des facteurs de risques vasculaires. Elle représente l’affection vasculaire rétinienne la plus fréquente après la rétinopathie diabétique et une cause importante de baisse de vision.
L’OVR se présente typiquement comme une baisse de vision unilatérale de survenue brutale, chez un sujet de plus de 50 ans.
![]() Trois sous-groupes principaux d’OVR peuvent être distingués en fonction de la localisation de l’obstruction :
Trois sous-groupes principaux d’OVR peuvent être distingués en fonction de la localisation de l’obstruction :
- • l’occlusion de la veine centrale de la rétine (OVCR), qui survient à proximité de la lame criblée du nerf optique;
- • l’occlusion d’une hémiveine centrale de la rétine (hémi-OVCR), qui s’apparente à une OVCR;
- • l’occlusion de branche veineuse rétinienne (OBVR), qui survient au niveau d’un croisement artérioveineux.
I 308Épidémiologie et facteurs de risque
La prévalence de l’OVCR est estimée de 0,1 % à 0,4 % et l’OBVR, plus fréquente, touche 0,6 % à 1,2 % des individus.
Le principal facteur de risque des OVR est l’âge. Celles-ci touchent de façon équivalente les hommes et les femmes.
![]() Les OVCR surviennent le plus souvent chez des sujets de plus de 50 ans (dans 75 % des cas après 60 ans) présentant des facteurs de risques cardiovasculaires et d’artériosclérose. En dehors de l’âge, d’autres facteurs de risque d’OVR, OVCR et OBVR, ont été identifiés :
Les OVCR surviennent le plus souvent chez des sujets de plus de 50 ans (dans 75 % des cas après 60 ans) présentant des facteurs de risques cardiovasculaires et d’artériosclérose. En dehors de l’âge, d’autres facteurs de risque d’OVR, OVCR et OBVR, ont été identifiés :
II Physiopathogénie
![]() L’OVCR est secondaire à une obstruction et/ou un ralentissement majeur du flux sanguin dans la veine centrale de la rétine au niveau de la tête du nerf optique.
L’OVCR est secondaire à une obstruction et/ou un ralentissement majeur du flux sanguin dans la veine centrale de la rétine au niveau de la tête du nerf optique.
Il est couramment admis que l’épaississement de la paroi de l’artère centrale de la rétine, athé-roscléreuse, pourrait entraîner une compression de la veine centrale adjacente et son occlusion. Une augmentation des résistances en arrière de la lame criblée pourrait aussi jouer un rôle.
Concernant les OBVR, l’artère et la veine partagent une gaine adventicielle commune à l’endroit des croisements artérioveineux. Presque toutes les OBVR sont une complication de l’artériosclérose et sont liées à un signe du croisement : elles sont le « stade + » du signe du croisement, liées à la compression de la veine rétinienne par la paroi épaissie de l’artère artérioscléreuse.
L’augmentation importante du taux de VEGF (vascular endothelialgrowth factor) intraoculaire joue également un rôle clé ainsi que pour la survenue d’un œdème maculaire.
III Signes fonctionnels
A Signes fonctionnels de l’OVCR
Le principal signe fonctionnel de l’OVCR est une baisse d’acuité visuelle brutale unilatérale. L’œil est blanc, indolore.
La baisse d’acuité visuelle est plus ou moins importante selon la forme de l’OVCR : ![]() l’acuité visuelle peut varier d’une simple perception lumineuse à une acuité visuelle normale. En effet, l’acuité visuelle est corrélée avec la qualité de perfusion du lit capillaire rétinien, et varie donc selon la sévérité de l’OVCR :
l’acuité visuelle peut varier d’une simple perception lumineuse à une acuité visuelle normale. En effet, l’acuité visuelle est corrélée avec la qualité de perfusion du lit capillaire rétinien, et varie donc selon la sévérité de l’OVCR :
La baisse d’acuité visuelle est due aux hémorragies, à l’ischémie ou à l’œdème maculaire.
B 309Signes fonctionnels de l’OBVR
![]() Une OBVR peut entraîner un déficit sectoriel du champ visuel, accompagné ou non d’une baisse d’acuité visuelle.
Une OBVR peut entraîner un déficit sectoriel du champ visuel, accompagné ou non d’une baisse d’acuité visuelle.
![]() Le retentissement visuel de l’OBVR dépend plus de sa topographie que de son étendue; ainsi, des occlusions de veines maculaires, même si elles ne concernent qu’un petit territoire, sont habituellement symptomatiques. À l’inverse, si le territoire de drainage de la veine occluse n’inclut pas la macula, l’acuité visuelle peut être normale.
Le retentissement visuel de l’OBVR dépend plus de sa topographie que de son étendue; ainsi, des occlusions de veines maculaires, même si elles ne concernent qu’un petit territoire, sont habituellement symptomatiques. À l’inverse, si le territoire de drainage de la veine occluse n’inclut pas la macula, l’acuité visuelle peut être normale.
IV Signes cliniques
L’aspect ophtalmoscopique est dominé par les signes liés à la gêne au retour veineux dans les veines rétiniennes confluant vers la papille.
A Examen du fond d’œil
![]() Au fond d’œil, les deux principaux signes de l’OVCR sont (fig. 17.4 et fig. 17.5) :
Au fond d’œil, les deux principaux signes de l’OVCR sont (fig. 17.4 et fig. 17.5) :

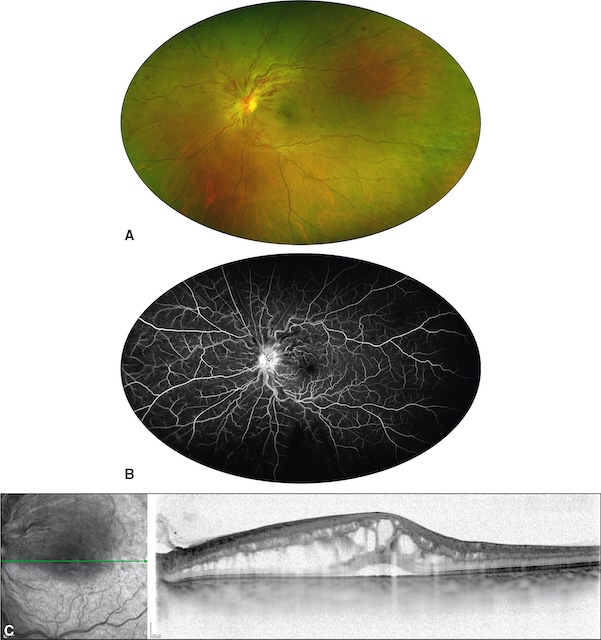
Dilatation et tortuosités veineuses, hémorragies en flammèches, hémorragies en taches disséminées. En angiographie (B), il n’y a pas de zones de non-perfusion étendues. En OCT (C), il existe un volumineux œdème maculaire.
L’image A en couleur montre un fond d’œil élargi avec une macula bombée et un nerf optique bien net, tandis que des reflets blanchâtres discrets évoquent un œdème rétinien. L’image B en angiographie à la fluorescéine révèle une hyperfluorescence maculaire diffuse avec imprégnation vasculaire progressive, traduisant une fuite vasculaire importante. En image C, la coupe OCT met en évidence un épaississement rétinien central avec de multiples cavités intrarétiniennes hypo-réflectives, caractéristiques d’un œdème maculaire cystoïde. L’ensemble des clichés suggère une atteinte maculaire exsudative d’origine vasculaire, probablement liée à une rétinopathie diabétique ou une occlusion veineuse.

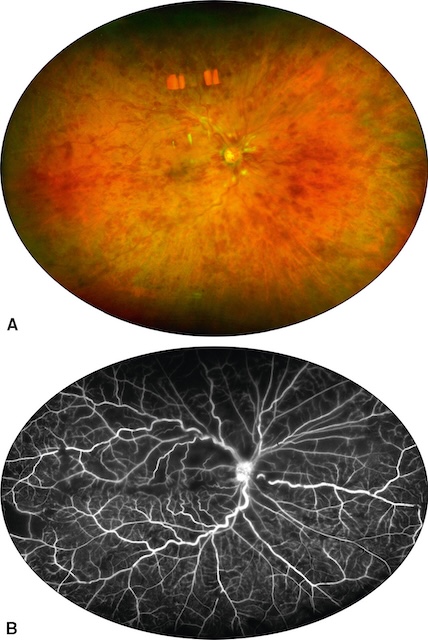
A. La rétinophotographie couleur retrouve la présence de très nombreuses hémorragies en taches et de nodules cotonneux. B. L’angiographie à la fluorescéine montre de multiples territoires non perfusés.
L’image A en fond d’œil montre un aspect diffusément hémorragique avec des hémorragies flammèches étendues sur toute la rétine, accompagnées d’un œdème maculaire discret et d’un flou péripapillaire. La présence de zones rétiniennes pâles avec des exsudats et des vaisseaux dilatés évoque un ralentissement du flux veineux. L’image B, en angiographie à la fluorescéine, révèle une importante non-perfusion capillaire dans les zones périphériques, traduisant une ischémie sévère. L’hyperfluorescence péripapillaire et maculaire suggère une fuite vasculaire active. Ces éléments sont typiques d’une occlusion de la veine centrale de la rétine dans sa forme ischémique.
![]() On peut également retrouver la présence :
On peut également retrouver la présence :
L’apparition d’une circulation collatérale au niveau du nerf optique peut être observée plusieurs mois ou années après la survenue de l’occlusion et est un signe de chronicité.
![]() Une hémi-occlusion veineuse rétinienne (hémi-OVCR) se présente avec les mêmes signes cliniques, mais ceux-ci ne touchent que la moitié de la rétine seulement, supérieure ou inférieure. Cette entité est considérée comme une variante d’OVCR, partageant un même tableau clinique, une évolution et des complications similaires.
Une hémi-occlusion veineuse rétinienne (hémi-OVCR) se présente avec les mêmes signes cliniques, mais ceux-ci ne touchent que la moitié de la rétine seulement, supérieure ou inférieure. Cette entité est considérée comme une variante d’OVCR, partageant un même tableau clinique, une évolution et des complications similaires.
![]() Les modifications du fond d’œil au cours des OBVR sont identiques à celles des OVCR, mais limitées au territoire drainé par la veine occluse : le territoire concerné par l’occlusion a une forme triangulaire correspondant au territoire drainé par la branche veineuse rétinienne en amont du croisement artérioveineux. Plus le croisement responsable de l’OBVR est proche de la papille, plus le territoire concerné est important.
Les modifications du fond d’œil au cours des OBVR sont identiques à celles des OVCR, mais limitées au territoire drainé par la veine occluse : le territoire concerné par l’occlusion a une forme triangulaire correspondant au territoire drainé par la branche veineuse rétinienne en amont du croisement artérioveineux. Plus le croisement responsable de l’OBVR est proche de la papille, plus le territoire concerné est important.
Au fond d’œil, on retrouvera donc une dilatation et une tortuosité veineuses, des hémorragies rétiniennes, des nodules cotonneux et un œdème rétinien, localisés au territoire rétinien normalement drainé par la veine occluse (fig. 17.6 et fig. 17.7).

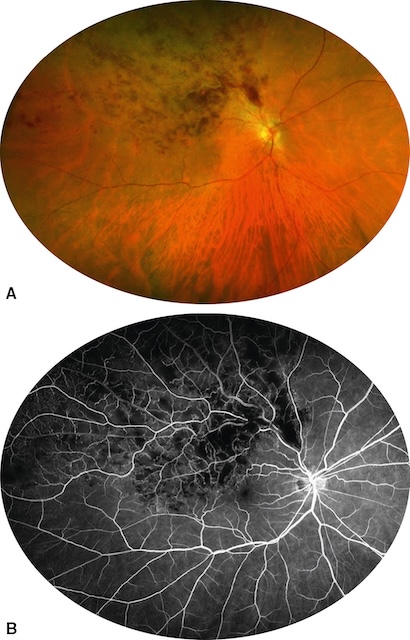
A. La rétinophotographie retrouve de nombreuses hémorragies en taches dans le territoire de la veine occluse. B. L’angiographie à la fluorescéine confirme la présence de zones non perfusées dans le territoire de l’occlusion.
L’image A, prise en fond d’œil, montre une hémorragie étendue au pôle supérieur de la rétine, suivant le trajet d’une branche veineuse temporale supérieure. On distingue une dilatation et une tortuosité des veines dans la zone concernée, ainsi qu’un œdème rétinien associé à une macula relativement épargnée. L’image B en angiographie à la fluorescéine révèle une vaste zone de non-perfusion dans le territoire affecté, avec de nombreuses anomalies de perfusion capillaire. On note également une hyperfluorescence diffuse traduisant une fuite vasculaire. Ces signes sont typiques d’une OBVR temporale supérieure à prédominance ischémique.

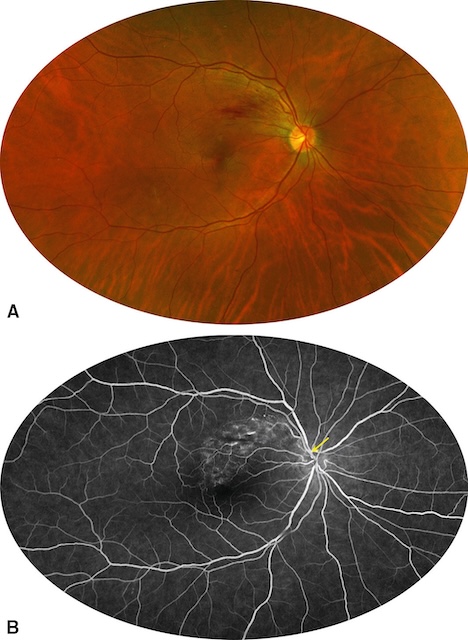
A. La rétinophotographie montre la présence d’hémorragies en flammèche dans le territoire occlus. B. L’angiographie à la fluorescéine montre que le territoire de l’occlusion reste bien perfusé. Une OBVR survient au niveau d’un croisement artérioveineux (flèche jaune). Elle est la conséquence de la compression de la veine par la paroi épaissie d’une artère artérioscléreuse.
Sur l’image A en fond d’œil, on observe une dilatation modérée et une tortuosité d’une branche veineuse temporale supérieure, avec quelques hémorragies intrarétiniennes diffuses dans le territoire drainé. Il n’y a pas de signes d’ischémie étendue ni d’œdème massif, ce qui traduit une forme plus modérée. L’image B, en angiographie à la fluorescéine, confirme l’absence de non-perfusion capillaire notable et montre une hyperfluorescence discrète au niveau de la veine affectée, liée à une fuite vasculaire légère. L’ensemble des signes évoque une OBVR à forme non ischémique, avec atteinte fonctionnelle modérée et risque évolutif plus limité.
L’apparition d’une circulation collatérale adjacente au territoire occlus peut être observée plusieurs mois ou années après la survenue de l’occlusion et est un signe de chronicité.
B Diagnostic positif
Le diagnostic positif d’une OVCR ou d’une OBVR repose uniquement sur l’examen clinique du fond d’œil dilaté.
En revanche, le diagnostic de la forme clinique, non ischémique ou ischémique, nécessite le plus souvent le recours à l’angiographie à la fluorescéine.
310Les formes non ischémiques sont les plus fréquentes – les trois quarts environ de l’ensemble des OVCR. On peut les apparenter à une stase veineuse rétinienne. L’acuité visuelle est habituellement supérieure à 2/10es; le réflexe pupillaire n’est pas modifié.
Au fond d’œil, les hémorragies ont une forme en flammèches (voir fig. 17.4), traduisant leur topographie dans les couches superficielles de la rétine, le long des fibres optiques. Il existe aussi souvent des hémorragies en taches. Les nodules cotonneux sont rares.
En angiographie, il existe une importante dilatation veineuse associée à des dilatations capillaires; les territoires d’ischémie rétinienne sont peu étendus.
311Les formes ischémiques représentent environ un quart des OVCR. On peut les apparenter à un infarcissement hémorragique de la rétine. Le diagnostic de la forme ischémique d’une OVCR repose sur la présence de nombreux territoires rétiniens non perfusés en angiographie à la fluorescéine (voir fig. 17.5).
![]() Cependant, l’évaluation de la perfusion rétinienne peut être difficile à la phase aiguë d’une OVCR en cas d’hémorragies rétiniennes nombreuses et étendues.
Cependant, l’évaluation de la perfusion rétinienne peut être difficile à la phase aiguë d’une OVCR en cas d’hémorragies rétiniennes nombreuses et étendues.
![]() D’autres éléments sont donc à rechercher en faveur du caractère ischémique d’une OVCR à la phase initiale :
D’autres éléments sont donc à rechercher en faveur du caractère ischémique d’une OVCR à la phase initiale :
- • une acuité visuelle effondrée, habituellement inférieure à 1/10e;
- • le réflexe pupillaire direct diminué = déficit pupillaire afférant (avec conservation du réflexe consensuel à l’éclairement de l’œil controlatéral sain);
- • 312les hémorragies nombreuses, volumineuses, profondes, « en taches » (voir fig. 17.5), témoins de l’ischémie rétinienne à l’examen du fond d’œil;
- • de nombreux nodules cotonneux à l’examen du fond d’œil (voir fig. 17.5);
- • la présence d’une néovascularisation irienne (voir plus loin « VII. Évolution »);
- • la présence de zones de non-perfusion capillaire rétinienne sur l’angiographie à la fluores-céine d’une taille supérieure à 10 diamètres papillaires;
- • des altérations de l’électrorétinogramme (par exemple réduction de l’amplitude de l’onde b, rapport d’onde b/a réduit, etc.), mais celui-ci est rarement réalisé en pratique.
313![]() Le passage d’une forme initialement non ischémique d’OVCR à une forme ischémique peut être observé (environ 30 % des formes non ischémiques au cours du suivi).
Le passage d’une forme initialement non ischémique d’OVCR à une forme ischémique peut être observé (environ 30 % des formes non ischémiques au cours du suivi).
![]() De la même façon, dans une OBVR, l’angiographie à la fluorescéine contribue à préciser la forme clinique : forme non ischémique (voir fig. 17.7) ou forme ischémique (voir fig. 17.6), comme dans les OVCR. L’imagerie en OCT-angiographie peut également permettre d’évaluer la perfusion capillaire du territoire occlus et de définir la forme ischémique ou non de l’OBVR (fig. 17.8).
De la même façon, dans une OBVR, l’angiographie à la fluorescéine contribue à préciser la forme clinique : forme non ischémique (voir fig. 17.7) ou forme ischémique (voir fig. 17.6), comme dans les OVCR. L’imagerie en OCT-angiographie peut également permettre d’évaluer la perfusion capillaire du territoire occlus et de définir la forme ischémique ou non de l’OBVR (fig. 17.8).

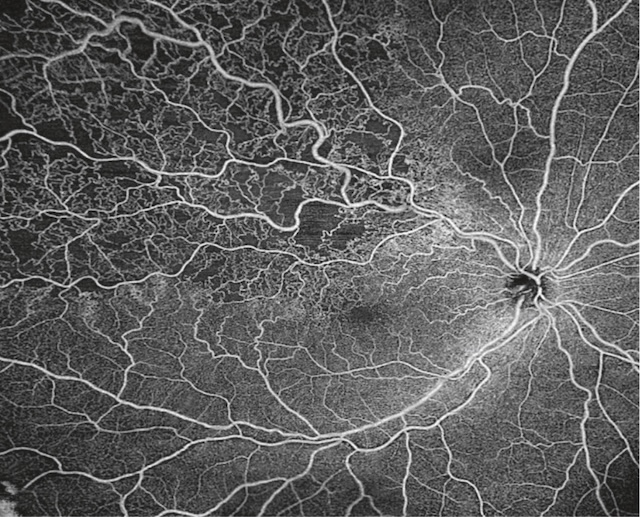
Cette image d’OCT-angiographie révèle une occlusion d’une branche veineuse rétinienne temporale supérieure avec des signes marqués d’ischémie. On distingue clairement une dilatation importante et une tortuosité des veines impliquées, tandis que les capillaires adjacents présentent de larges zones de non-perfusion. L’architecture vasculaire est désorganisée, notamment dans la moitié supérieure gauche de l’image où le réseau capillaire est visiblement interrompu, traduisant une perte significative de vascularisation. Le contraste entre les zones bien perfusées et les zones ischémiques est net, suggérant une atteinte sévère du drainage veineux dans ce secteur de la rétine.
V 314Examens complémentaires ophtalmologiques
L’angiographie à la fluorescéine est réalisée pour rechercher des territoires non perfusés et différencier les formes non ischémiques des formes ischémiques. ![]() Elle peut être pratiquée soit d’emblée, soit secondairement après diminution du nombre et de l’étendue des hémorragies. Elle peut être répétée au cours du suivi en cas de suspicion d’aggravation d’une forme initialement non ischémique.
Elle peut être pratiquée soit d’emblée, soit secondairement après diminution du nombre et de l’étendue des hémorragies. Elle peut être répétée au cours du suivi en cas de suspicion d’aggravation d’une forme initialement non ischémique.
![]() La tomographie en cohérence optique (OCT) est réalisée dans le bilan initial, pour diagnostiquer et quantifier l’œdème maculaire. Par la suite, elle permettra de suivre l’évolution de l’œdème maculaire au cours du traitement.
La tomographie en cohérence optique (OCT) est réalisée dans le bilan initial, pour diagnostiquer et quantifier l’œdème maculaire. Par la suite, elle permettra de suivre l’évolution de l’œdème maculaire au cours du traitement.
Si elle est disponible, une OCT-angiographie peut également être réalisée afin d’évaluer de façon non invasive la perfusion capillaire rétinienne.
VI Bilan étiologique
![]() Les OVCR surviennent le plus souvent chez des sujets de plus de 50 ans présentant des facteurs de risques cardiovasculaires.
Les OVCR surviennent le plus souvent chez des sujets de plus de 50 ans présentant des facteurs de risques cardiovasculaires.
Chez le sujet de plus de 50 ans, le bilan étiologique se résume donc le plus souvent à la recherche de facteurs de risques cardiovasculaires : tabagisme, HTA, diabète, hypercholestérolémie.
Le contrôle de la pression artérielle, ou, au mieux, la réalisation d’un Holter tensionnel sur 24 heures sont généralement associés à la prescription d’un bilan sanguin minimal (glycémie à jeun, bilan lipidique, NFS, VS, CRP).
![]() La recherche d’une hypertonie oculaire et d’un glaucome primitif à angle ouvert (voir chapitre 14) doit également être systématique.
La recherche d’une hypertonie oculaire et d’un glaucome primitif à angle ouvert (voir chapitre 14) doit également être systématique.
Une approche multidisciplinaire doit être réalisée chez les patients atteints d’OVR en collaboration avec le médecin traitant, sur les antécédents médicaux et l’examen physique approfondi. Le bilan biologique doit être guidé par antécédents médicaux et par la détection de signes 315cliniques atypiques. Chez les patients âgés de moins de 50 ans, sans facteurs de risque, un bilan complémentaire de thrombophilie recherche :
VII Évolution
![]() L’évolution des occlusions veineuses dépend de la forme clinique.
L’évolution des occlusions veineuses dépend de la forme clinique.
Les deux complications occlusions veineuses sont l’œdème maculaire et la néovascularisation.
A Évolution des OVCR
![]() L’acuité est généralement faible (< 5/10es) dans l’OVCR à la phase aiguë et, en l’absence de traitement, elle tend à diminuer avec le temps. L’acuité visuelle initiale est un bon facteur prédictif de l’acuité visuelle à 3 ans dans l’OVCR. Il a été démontré que le résultat visuel est fortement dépendant de l’étendue de la non-perfusion capillaire rétinienne.
L’acuité est généralement faible (< 5/10es) dans l’OVCR à la phase aiguë et, en l’absence de traitement, elle tend à diminuer avec le temps. L’acuité visuelle initiale est un bon facteur prédictif de l’acuité visuelle à 3 ans dans l’OVCR. Il a été démontré que le résultat visuel est fortement dépendant de l’étendue de la non-perfusion capillaire rétinienne.
1 Formes non ischémiques
![]() Les OVCR non ischémiques ont une évolution favorable dans la moitié des cas, avec une normalisation de l’acuité visuelle et de l’aspect du fond d’œil en 3 à 6 mois. L’évolution est parfois moins favorable :
Les OVCR non ischémiques ont une évolution favorable dans la moitié des cas, avec une normalisation de l’acuité visuelle et de l’aspect du fond d’œil en 3 à 6 mois. L’évolution est parfois moins favorable :
- •
 soit par conversion en une forme ischémique (environ un quart des cas);
soit par conversion en une forme ischémique (environ un quart des cas); - • soit par la persistance d’un œdème maculaire, responsable d’une baisse d’acuité visuelle permanente :
 l’œdème maculaire après OVCR est dû à l’altération des capillaires macu-laires qui laissent diffuser du liquide dans la rétine. Cet œdème maculaire peut persister de façon prolongée, malgré la régression de la dilatation veineuse. En l’absence de traitement, l’œdème maculaire chronique peut entraîner des altérations rétiniennes irréversibles au niveau maculaire, conduisant à une baisse d’acuité visuelle irréversible.
l’œdème maculaire après OVCR est dû à l’altération des capillaires macu-laires qui laissent diffuser du liquide dans la rétine. Cet œdème maculaire peut persister de façon prolongée, malgré la régression de la dilatation veineuse. En l’absence de traitement, l’œdème maculaire chronique peut entraîner des altérations rétiniennes irréversibles au niveau maculaire, conduisant à une baisse d’acuité visuelle irréversible.
2 Formes ischémiques
![]() Les formes ischémiques (d’emblée ou secondairement) sont de pronostic beaucoup plus sévère. L’acuité visuelle est d’emblée effondrée, habituellement inférieure à 1/10e, sans espoir de récupération fonctionnelle du fait de l’ischémie maculaire majeure.
Les formes ischémiques (d’emblée ou secondairement) sont de pronostic beaucoup plus sévère. L’acuité visuelle est d’emblée effondrée, habituellement inférieure à 1/10e, sans espoir de récupération fonctionnelle du fait de l’ischémie maculaire majeure.
![]() Cette ischémie rétinienne étendue peut entraîner l’apparition d’une néovascularisation rétinienne et irienne.
Cette ischémie rétinienne étendue peut entraîner l’apparition d’une néovascularisation rétinienne et irienne.
Le développement d’une néovascularisation irienne, ou rubéose irienne (fig. 17.9), est la complication la plus redoutable des OVCR de type ischémique par son risque d’évolution rapide vers un glaucome néovasculaire (GNV). En cas d’ischémie rétinienne étendue, des néovaisseaux se développent à la surface de l’iris et au niveau de l’angle iridocornéen, créant alors un blocage 316de l’écoulement de l’humeur aqueuse à travers le trabeculum. Ce blocage entraîne une augmentation brutale de la pression intraoculaire caractérisant le stade de GNV.

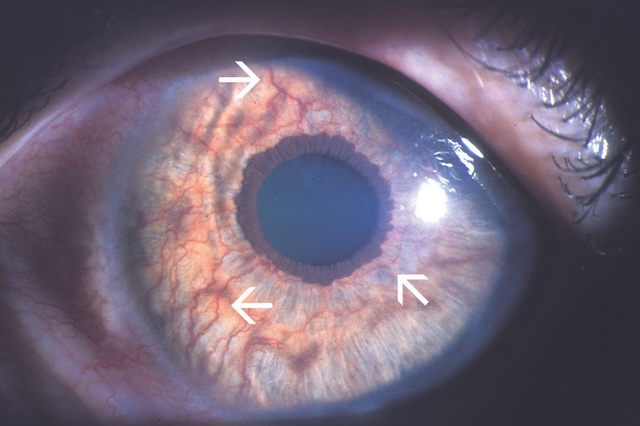
Présence sur la face antérieure de l’iris de nombreux vaisseaux anormalement visibles (flèches).
Cette photographie en lumière focalisée montre un œil en gros plan, révélant une néovascularisation irienne. De fins vaisseaux sanguins anormaux apparaissent à la surface de l’iris, formant un réseau dense et désorganisé, principalement situé autour de la pupille et dans le stroma irien moyen. Ces vaisseaux sont bien visibles, serpentant à travers la trame pigmentaire de l’iris, contrastant avec sa teinte brune et orangée. La lumière incidente accentue leur relief et leur irrégularité. L’aspect global de l’œil, avec une pupille bien dilatée et une cornée claire, souligne davantage la présence pathologique de ces structures vasculaires superficielles.
La présence d’une rubéose irienne peut aussi se compliquer d’un hyphema (= présence de sang dans la chambre antérieure de l’œil), par saignement des néovaisseaux iriens.
La néovascularisation irienne peut survenir très rapidement, en quelques jours ou quelques semaines après une OVCR ischémique, et aboutir à un GNV dès le 3e mois. Cette évolution spontanée rapide vers le GNV doit être prévenue par un traitement laser de la rétine ischémique, la photocoagulation panrétinienne, mise en route dès le diagnostic d’une forme ischémique d’OVCR.
![]() Chez les patients traités par injections d’anti-VEGF, ceux-ci ayant des effets anti-angiogéniques limitant la croissance des néovaisseaux, la survenue du GNV peut être retardée et survenir 1 à 2 ans après le début de l’OVCR.
Chez les patients traités par injections d’anti-VEGF, ceux-ci ayant des effets anti-angiogéniques limitant la croissance des néovaisseaux, la survenue du GNV peut être retardée et survenir 1 à 2 ans après le début de l’OVCR.
![]() La néovascularisation prérétinienne et/ou prépapillaire est retrouvée dans 25 % des cas d’OVCR ischémique. Son mécanisme d’apparition est similaire à celui de la rétinopathie diabétique proliférante (voir chapitre 20); elle peut se compliquer d’hémorragie intravitréenne, responsable d’une baisse d’acuité visuelle brutale et/ou de myodésopsies.
La néovascularisation prérétinienne et/ou prépapillaire est retrouvée dans 25 % des cas d’OVCR ischémique. Son mécanisme d’apparition est similaire à celui de la rétinopathie diabétique proliférante (voir chapitre 20); elle peut se compliquer d’hémorragie intravitréenne, responsable d’une baisse d’acuité visuelle brutale et/ou de myodésopsies.
![]() Une surveillance régulière de l’acuité visuelle, de l’iris et du fond d’œil est donc nécessaire pour évaluer les signes d’ischémie.
Une surveillance régulière de l’acuité visuelle, de l’iris et du fond d’œil est donc nécessaire pour évaluer les signes d’ischémie.
B Évolution des OBVR
Dans la majorité des cas, l’évolution anatomique est spontanément favorable par reperméabi-lisation de la veine rétinienne ou par développement d’une circulation de suppléance permettant le drainage du territoire de l’OBVR par une veine rétinienne de voisinage.
Concernant l’évolution de l’acuité visuelle, l’acuité initiale varie entre 5/10es et < 1/10e dans les OBVR, et même si une guérison partielle spontanée peut survenir, une amélioration de l’acuité visuelle au-delà de 5/10es est rare.
2 Évolution défavorable
![]() L’évolution peut être défavorable du fait soit :
L’évolution peut être défavorable du fait soit :
- • d’une maculopathie ischémique, au cours d’une forme ischémique intéressant la macula;
- • d’un œdème maculaire persistant, de la même façon que dans les OVCR, mais moins sévère car sectoriel, limité au territoire maculaire intéressé par l’occlusion veineuse;
- • 317de néovaisseaux prérétiniens secondaires à une forme ischémique suffisamment étendue; ceux-ci peuvent rarement entraîner la survenue d’une hémorragie du vitré, responsable d’une baisse d’acuité visuelle brutale dans les mois suivant la survenue de l’occlusion.
 L’ischémie rétinienne des OBVR n’est en revanche pas suffisamment étendue pour provoquer l’apparition de néovaisseaux prépapillaires ou d’une néovascularisation irienne et d’un GNV.
L’ischémie rétinienne des OBVR n’est en revanche pas suffisamment étendue pour provoquer l’apparition de néovaisseaux prépapillaires ou d’une néovascularisation irienne et d’un GNV.
VIII Traitement
![]() Le but du traitement d’une occlusion veineuse est principalement d’éviter ou de traiter les complications :
Le but du traitement d’une occlusion veineuse est principalement d’éviter ou de traiter les complications :
A Méthodes
Le traitement médical des occlusions veineuses repose uniquement sur la prise en charge des facteurs de risques cardiovasculaires.
![]() Aucun traitement médical n’a prouvé son efficacité dans la prise en charge des occlusions veineuses rétiniennes.
Aucun traitement médical n’a prouvé son efficacité dans la prise en charge des occlusions veineuses rétiniennes.
- • Anticoagulants. Ils n’ont pas d’efficacité prouvée et ne sont pas indiqués en dehors des rares cas d’anomalie de la coagulation.
- • Fibrinolytiques. Ils ont été utilisés dans le but de dissoudre un éventuel thrombus, soit par voie générale, soit par injection directe dans l’artère ophtalmique; le bénéfice de ces traitements, quelle que soit la voie d’administration, est difficile à prouver et, compte tenu de leurs risques de complications, ils ne sont pas indiqués dans la pratique courante.
- • Hémodilution isovolémique. Le principe de l’hémodilution isovolémique est de diminuer la viscosité sanguine et donc d’améliorer la circulation veineuse rétinienne en abaissant l’hématocrite entre 30 % et 35 %; son efficacité est discutée.
- • Antiagrégants plaquettaires. Ils ont été proposés, mais n’ont pas fait la preuve de leur efficacité dans le traitement des OVCR.
2 Traitements par injections intravitréennes
![]() Le traitement de l’œdème maculaire repose sur les injections intravitréennes d’anti-VEGF (ranibizumab ou aflibercept) ou de corticoïdes (implant de dexaméthasone) qui ont fait la preuve de leur efficacité pour améliorer l’acuité visuelle dans cette indication. Ils permettent de réduire les diffusions de liquide à partir des capillaires maculaires altérés. Ces traitements nécessitent le plus souvent des injections répétées pendant plusieurs mois voire plusieurs années.
Le traitement de l’œdème maculaire repose sur les injections intravitréennes d’anti-VEGF (ranibizumab ou aflibercept) ou de corticoïdes (implant de dexaméthasone) qui ont fait la preuve de leur efficacité pour améliorer l’acuité visuelle dans cette indication. Ils permettent de réduire les diffusions de liquide à partir des capillaires maculaires altérés. Ces traitements nécessitent le plus souvent des injections répétées pendant plusieurs mois voire plusieurs années.
![]() Les injections d’anti-VEGF ne sont pas recommandées chez les patients ayant eu un événement cardiovasculaire récent. L’injection d’un implant de dexaméthasone peut se compliquer, comme toute corticothérapie, d’une cataracte ou d’une augmentation de la pression intraoculaire.
Les injections d’anti-VEGF ne sont pas recommandées chez les patients ayant eu un événement cardiovasculaire récent. L’injection d’un implant de dexaméthasone peut se compliquer, comme toute corticothérapie, d’une cataracte ou d’une augmentation de la pression intraoculaire.
3 Photocoagulation au laser
![]() Son principe est similaire à la photocoagulation dans la rétinopathie diabétique (voir chapitre 20).
Son principe est similaire à la photocoagulation dans la rétinopathie diabétique (voir chapitre 20).
318La photocoagulation panrétinienne (PPR) est indiquée dans les formes ischémiques d’OVCR.
![]() Elle vise à détruire les territoires ischémiques pour réduire la consommation en oxygène de la rétine (et ainsi réduire la production locale de VEGF), afin d’éviter ou de faire régresser la néovascularisation. L’ensemble de la rétine périphérique doit être traitée par laser pour permettre de faire régresser la néovascularisation de façon définitive.
Elle vise à détruire les territoires ischémiques pour réduire la consommation en oxygène de la rétine (et ainsi réduire la production locale de VEGF), afin d’éviter ou de faire régresser la néovascularisation. L’ensemble de la rétine périphérique doit être traitée par laser pour permettre de faire régresser la néovascularisation de façon définitive.
![]() De même, la photocoagulation sectorielle des zones d’ischémie rétinienne dans le territoire de l’occlusion est réalisée dans les formes ischémiques d’OBVR pour éviter la survenue d’une hémorragie du vitré par néovaisseaux prérétiniens.
De même, la photocoagulation sectorielle des zones d’ischémie rétinienne dans le territoire de l’occlusion est réalisée dans les formes ischémiques d’OBVR pour éviter la survenue d’une hémorragie du vitré par néovaisseaux prérétiniens.
![]() Bien qu’ayant un mécanisme d’action anti-angiogénique, les anti-VEGF ne sont pas indiqués dans le traitement de l’ischémie rétinienne (mais uniquement indiqués pour le traitement de l’œdème maculaire) en raison de leur courte durée d’action : ils permettent une régression simplement transitoire et non définitive de la néovascularisation.
Bien qu’ayant un mécanisme d’action anti-angiogénique, les anti-VEGF ne sont pas indiqués dans le traitement de l’ischémie rétinienne (mais uniquement indiqués pour le traitement de l’œdème maculaire) en raison de leur courte durée d’action : ils permettent une régression simplement transitoire et non définitive de la néovascularisation.
B Indications
![]() Les injections intravitréennes d’anti-VEGF ou d’implant de dexaméthasone peuvent être proposées en présence d’un œdème maculaire avec baisse d’acuité visuelle.
Les injections intravitréennes d’anti-VEGF ou d’implant de dexaméthasone peuvent être proposées en présence d’un œdème maculaire avec baisse d’acuité visuelle.
![]() Dans tous les cas, une surveillance clinique et angiographique tous les mois au début permettra de déceler précocement la conversion vers une forme ischémique.
Dans tous les cas, une surveillance clinique et angiographique tous les mois au début permettra de déceler précocement la conversion vers une forme ischémique.
2 Formes ischémiques
![]() Un traitement par PPR doit être pratiqué d’emblée lorsque l’ischémie est très étendue, C sans attendre l’apparition de la néovascularisation irienne. Le patient doit être informé que le but du traitement n’est pas de rétablir la vision mais d’éviter l’évolution vers le GNV.
Un traitement par PPR doit être pratiqué d’emblée lorsque l’ischémie est très étendue, C sans attendre l’apparition de la néovascularisation irienne. Le patient doit être informé que le but du traitement n’est pas de rétablir la vision mais d’éviter l’évolution vers le GNV.
![]() Les injections intravitréennes d’anti-VEGF ou d’implant de dexaméthasone peuvent également être proposées en présence d’un œdème maculaire associé.
Les injections intravitréennes d’anti-VEGF ou d’implant de dexaméthasone peuvent également être proposées en présence d’un œdème maculaire associé.
3 Glaucome néovasculaire
Si un GNV est déjà installé, la PPR doit être réalisée en urgence, après avoir fait baisser la pression intraoculaire par un traitement hypotonisant local et de l’acétazolamide ![]() (Diamox®) per os ou par voie intraveineuse. Une intervention chirurgicale à visée hypotonisante peut être nécessaire dans les cas les plus graves.
(Diamox®) per os ou par voie intraveineuse. Une intervention chirurgicale à visée hypotonisante peut être nécessaire dans les cas les plus graves.
Les injections d’anti-VEGF peuvent être utilisées en traitement adjuvant pour permettre une régression partielle de la rubéose irienne en attendant l’efficacité du laser.
 Compléments en ligne
Compléments en ligne
Concernant l’occlusion de la veine centrale de la rétine, quel(s) examen(s) complémentaire(s) ophtalmologique(s) permettrai(en)t de mieux en préciser la forme ?
Quelle(s) est (sont) la (les) complication(s) évolutive(s) potentielle(s) d’une occlusion de la veine centrale de la rétine ischémique ?
