CHAPITRE 6: Items 83 et 187 Infections et inflammations oculaires
Situations cliniques de départ
Les infections et inflammations oculaires peuvent être évoquées dans les situations cliniques suivantes.
 16 – Adénopathies uniques ou multiples : association possible avec certaines infections (par exemple bartonellose) et inflammations oculaires (par exemple sarcoïdose).
16 – Adénopathies uniques ou multiples : association possible avec certaines infections (par exemple bartonellose) et inflammations oculaires (par exemple sarcoïdose).
 34 – Douleur aiguë postopératoire : douleur aiguë associée à une endophtalmie postopératoire.
34 – Douleur aiguë postopératoire : douleur aiguë associée à une endophtalmie postopératoire.
 35 – Douleur chronique : douleur chronique post-zostérienne ophtalmique.
35 – Douleur chronique : douleur chronique post-zostérienne ophtalmique.
 62 – Trouble de la déglutition et fausse route : dysphagie dans le cadre d’une pemphi-goïde cicatricielle.
62 – Trouble de la déglutition et fausse route : dysphagie dans le cadre d’une pemphi-goïde cicatricielle.
 78 – Acné : sécheresse oculaire associée au traitement de l’acné par isotrétinoïne.
78 – Acné : sécheresse oculaire associée au traitement de l’acné par isotrétinoïne.
 82 – Bulle, éruption bulleuse : conjonctivites associées au maladies bulleuses.
82 – Bulle, éruption bulleuse : conjonctivites associées au maladies bulleuses.
 93 – Vésicules, éruption vésiculeuse (cutanéomuqueuse) : association possible avec certaines infections (par exemple herpès) et inflammations oculaires (par exemple maladies bulleuses).
93 – Vésicules, éruption vésiculeuse (cutanéomuqueuse) : association possible avec certaines infections (par exemple herpès) et inflammations oculaires (par exemple maladies bulleuses).
 127 – Paralysie faciale : kératopathie d’exposition associée à la paralysie faciale.
127 – Paralysie faciale : kératopathie d’exposition associée à la paralysie faciale.
 138 – Anomalie de la vision : association fréquente avec des infections et inflammations oculaires.
138 – Anomalie de la vision : association fréquente avec des infections et inflammations oculaires.
 139 – Anomalies palpébrales : sources habituelles d’infections et d’inflammations oculaires.
139 – Anomalies palpébrales : sources habituelles d’infections et d’inflammations oculaires.
 141 – Sensation de brûlure oculaire : un des symptômes des conjonctivites.
141 – Sensation de brûlure oculaire : un des symptômes des conjonctivites.
 151 – œdème de la face et du cou : les infections et inflammations de la surface oculaire peuvent s’accompagner d’un œdème palpébral et péri-orbitaire.
151 – œdème de la face et du cou : les infections et inflammations de la surface oculaire peuvent s’accompagner d’un œdème palpébral et péri-orbitaire.
 152 – œil rouge et/ou douloureux : signes d’appels principaux des infections et inflammations oculaires.
152 – œil rouge et/ou douloureux : signes d’appels principaux des infections et inflammations oculaires.
 155- Rhinorrhée : conjonctivites associées aux rhinorrhées allergiques ou infectieuses. 168 – Brûlure : source d’infections et d’inflammations oculaires.
155- Rhinorrhée : conjonctivites associées aux rhinorrhées allergiques ou infectieuses. 168 – Brûlure : source d’infections et d’inflammations oculaires.
 169 – Morsures et piqûres : sources d’infections et d’inflammations oculaires.
169 – Morsures et piqûres : sources d’infections et d’inflammations oculaires.
 170 – Plaie : source d’infections et d’inflammations oculaires.
170 – Plaie : source d’infections et d’inflammations oculaires.
 174 – Traumatisme facial : source d’infections et d’inflammations oculaires.
174 – Traumatisme facial : source d’infections et d’inflammations oculaires.
 178 – Demande/prescription raisonnée et choix d’un examen diagnostique : s’intègre dans l’enquête diagnostique des infections et inflammations oculaires.
178 – Demande/prescription raisonnée et choix d’un examen diagnostique : s’intègre dans l’enquête diagnostique des infections et inflammations oculaires.
 110186 – Syndrome inflammatoire aigu ou chronique : association possible avec certaines infections (par exemple infections systémiques) et inflammations oculaires (par exemple maladies inflammatoires systémiques).
110186 – Syndrome inflammatoire aigu ou chronique : association possible avec certaines infections (par exemple infections systémiques) et inflammations oculaires (par exemple maladies inflammatoires systémiques).
 203 – Élévation de la protéine C réactive (CRP) : association possible avec certaines infections et inflammations oculaires.
203 – Élévation de la protéine C réactive (CRP) : association possible avec certaines infections et inflammations oculaires.
 223 – Interprétation de l’hémogramme : s’intègre dans l’enquête diagnostique des infections et inflammations oculaires.
223 – Interprétation de l’hémogramme : s’intègre dans l’enquête diagnostique des infections et inflammations oculaires.
 235 – Découverte, diagnostic positif, dépistage rapide VIH : possible dans certaines atteintes infectieuses oculaires (par exemple uvéite syphilitique, rétinite à cytoméga-lovirus, conjonctivite à Chlamydia).
235 – Découverte, diagnostic positif, dépistage rapide VIH : possible dans certaines atteintes infectieuses oculaires (par exemple uvéite syphilitique, rétinite à cytoméga-lovirus, conjonctivite à Chlamydia).
 236 – Interprétation d’un résultat de sérologie : s’intègre dans l’enquête diagnostique des infections et inflammations oculaires.
236 – Interprétation d’un résultat de sérologie : s’intègre dans l’enquête diagnostique des infections et inflammations oculaires.
 249 – Prescrire des anti-inflammatoires non stéroïdiens (AINS) : s’intègre dans la prise en charge de certaines atteintes inflammatoires oculaires (par exemple sclérite).
249 – Prescrire des anti-inflammatoires non stéroïdiens (AINS) : s’intègre dans la prise en charge de certaines atteintes inflammatoires oculaires (par exemple sclérite).
 251 – Prescrire des corticoïdes par voie générale ou locale : s’intègre dans la prise en charge des atteintes oculaires inflammatoires et parfois des atteintes infectieuses.
251 – Prescrire des corticoïdes par voie générale ou locale : s’intègre dans la prise en charge des atteintes oculaires inflammatoires et parfois des atteintes infectieuses.
 311 – Prévention des infections liées aux soins : en ophtalmologie médicale (par exemple contagiosité de conjonctivites virales, risque infectieux lors des injections intravitréennes) ou chirurgicale (par exemple infections postopératoires).
311 – Prévention des infections liées aux soins : en ophtalmologie médicale (par exemple contagiosité de conjonctivites virales, risque infectieux lors des injections intravitréennes) ou chirurgicale (par exemple infections postopératoires).
 328 – Annonce d’une maladie chronique : de nombreuses infections et inflammations oculaires ont des présentations chroniques (par exemple uvéite de l’arthrite juvénile idiopathique) ou récurrentes (par exemple uvéite liée au terrain HLA-B27).
328 – Annonce d’une maladie chronique : de nombreuses infections et inflammations oculaires ont des présentations chroniques (par exemple uvéite de l’arthrite juvénile idiopathique) ou récurrentes (par exemple uvéite liée au terrain HLA-B27).
 352 – Expliquer un traitement au patient (adulte/enfant/adolescent) : les infections et inflammations oculaires concernent des patients de tous âges.
352 – Expliquer un traitement au patient (adulte/enfant/adolescent) : les infections et inflammations oculaires concernent des patients de tous âges.
Hiérarchisation des connaissances
| Rang | Rubrique | Intitulé et descriptif |
|
|
Identifier une urgence | Savoir reconnaître une anaphylaxie |
|
|
Pré+valence, épidémiologie | Connaître la fréquence et les facteurs aggravants de la sécheresse oculaire |
|
|
Physiopathologie | Bases physiopathologiques de l’urticaire |
|
|
Physiopathologie | Connaître les facteurs responsables de l’atopie : facteurs génétiques, immunologiques et environnementaux |
|
|
Physiopathologie | Physiopathologie de l’eczéma de contact |
|
|
Définition | Définition de l’urticaire |
|
|
Diagnostic positif | Connaître les signes de l’interrogatoire et de l’examen clinique : mode d’apparition/caractéristiques/rechercher baisse d’acuité visuelle/antécédents et notion de traumatisme; acuité visuelle/examen de la conjonctive, cornée, iris; chambre antérieure, conjonctive palpébrale |
|
|
Diagnostic positif | Hémorragie sous-conjonctivale : sémiologie/étiologies |
|
|
Diagnostic positif | Conjonctivite : sémiologie/étiologies/traitement |
|
|
Diagnostic positif | Kératite : sémiologie/étiologies/traitement |
|
|
Diagnostic positif | Uvéites (uvéite antérieure, postérieure ou panuvéite) : sémiologie/étiologies |
|
|
Diagnostic positif | Épisclérite, sclérite : sémiologie/étiologies/traitement |
|
|
Diagnostic positif | Connaître les signes cliniques d’un eczéma aigu |
|
|
Diagnostic positif | Savoir diagnostiquer une urticaire superficielle et profonde |
|
|
Diagnostic positif | Connaître les aspects cliniques de la dermatite atopique en fonction du stade et son mode évolutif |
|
|
Étiologies | Connaître les principales causes de l’urticaire : urticaires physique, de contact, alimentaires, médicamenteuses, infectieuses |
|
|
Étiologies | Connaître la démarche diagnostique étiologique dans un eczéma de contact et les principaux allergènes responsables |
|
|
Prise en charge | Conduite à tenir devant un œil rouge douloureux sans baisse d’acuité visuelle : hémorragie sous-conjonctivale/conjonctivite/épisclérite, sclérite |
|
|
Prise en charge | Connaître les indications et contre-indications des collyres anesthésiques, antibiotiques et corticoïdes |
|
|
Prise en charge | Connaître le traitement d’une urticaire aiguë |
|
|
Prise en charge | Connaître les grands principes du traitement de la dermatite atopique |
|
|
Prise en charge | Connaître les grands principes du traitement d’un eczéma de contact |
|
|
Prise en charge | Conduite à tenir devant un œil rouge douloureux avec BAV : kératite/uvéite antérieure/glaucome aigu GFA/infection postopératoire |
|
|
Prise en charge | Connaître les traitements de la sécheresse oculaire |
|
|
Suivi et/ou pronostic | Connaître les principales complications de la dermatite atopique |
|
|
Examens complémentaires | Prélèvement conjonctival : dans le cade de conjonctivite sévère ou kératite |
|
|
Examens complémentaires | Connaître le principe, la technique et l’interprétation des tests épicutanés |
|
|
Examens complémentaires | Connaître les examens complémentaires à réaliser pour le diagnostic d’une trichomonose, d’une infection à Chlamidia trachomatis et Neisseria gonorrhoeae |
|
|
Contenu multimédia | Savoir reconnaître une urticaire : photo de plaques œdémateuses d’urticaire |
|
|
Contenu multimédia | Savoir reconnaître une dermatite atopique : photo d’une dermatite atopique du nourrisson en poussée |
|
|
Contenu multimédia | Savoir reconnaître un eczéma aigu : photo d’un eczéma aigu |
I Introduction
![]() Les infections et inflammations oculaires sont un motif fréquent de consultation en ophtalmologie. Dans ces situations, c’est habituellement l’apparition ou le constat d’un œil rouge plus ou moins douloureux qui constitue le signe d’alerte important et qui amène à consulter. Face à ce tableau clinique, le défi pour le clinicien sera de savoir distinguer ce qui n’est pas inflammatoire, de repérer l’infection qui requiert de principe un traitement spécifique et, surtout, de différencier une pathologie bénigne d’une pathologie grave qui menace la fonction visuelle et nécessite une prise en charge urgente (glaucome aigu par fermeture de l’angle, infection postopératoire, corps étranger intraoculaire [CEIO], uvéite, kératite aiguë).
Les infections et inflammations oculaires sont un motif fréquent de consultation en ophtalmologie. Dans ces situations, c’est habituellement l’apparition ou le constat d’un œil rouge plus ou moins douloureux qui constitue le signe d’alerte important et qui amène à consulter. Face à ce tableau clinique, le défi pour le clinicien sera de savoir distinguer ce qui n’est pas inflammatoire, de repérer l’infection qui requiert de principe un traitement spécifique et, surtout, de différencier une pathologie bénigne d’une pathologie grave qui menace la fonction visuelle et nécessite une prise en charge urgente (glaucome aigu par fermeture de l’angle, infection postopératoire, corps étranger intraoculaire [CEIO], uvéite, kératite aiguë).
II Examen d’un œil rouge
![]() L’interrogatoire a pour objectif de :
L’interrogatoire a pour objectif de :
- • préciser le mode d’apparition et les caractéristiques de la rougeur oculaire :
- – premier épisode ou événement récurrent,
- – survenue récente ou ancienne (évolution aiguë ou chronique), installation brutale ou progressive, d’emblée ou avec un intervalle libre par rapport à un événement local ou général identifié,
- – unilatérale ou bilatérale soit d’emblée, soit de manière séquentielle;
- • préciser la notion de douleur, son type et son intensité :
- – douleurs superficielles : modérées, à type de sensation de corps étranger (poussières ou grains de sable), de picotements ou de brûlures, voire de démangeaisons, évoquant une conjonctivite, ou plus importantes, accompagnées d’une photophobie, d’un larmoiement et d’un blépharospasme évoquant une kératite aiguë,
- – douleurs plus profondes, de type ciliaire : modérées, évoquant une uvéite antérieure ou une épisclérite, ou intenses, avec des irradiations dans le territoire du trijumeau évoquant une sclérite ou un glaucome aigu;
- • rechercher une baisse d’acuité visuelle : l’absence de baisse d’acuité visuelle oriente vers une conjonctivite, une hémorragie sous-conjonctivale, plus rarement une tumeur de la surface oculaire (e-fig. 6.1) ou encore une épisclérite;
- • préciser les antécédents ophtalmologiques et généraux, les traitements en cours, notamment topiques, l’âge et la profession du patient;
- • rechercher une notion de traumatisme et les conditions de survenue (accident domestique ou du travail);
- • 113rechercher les signes associés locaux (prurit, sécrétions, etc.), régionaux (exophtalmie, œdème orbitaire et palpébral, adénopathies, etc.) et généraux (céphalées, fièvre, manifestations ORL, etc.).
B Examen clinique oculaire
L’examen est bilatéral et comparatif. Trois niveaux d’examen physique sont à considérer selon l’équipement à disposition : examen externe en lumière ambiante et avec une source lumineuse additionnelle, examen à l’aide d’un système grossissant couramment disponible pour faciliter l’analyse (optique type loupe ou numérique type tablette ou smartphone) et examen ophtalmologique à la lampe à fente.
2 Conjonctive bulbaire et paroi du globe
L’asnect, l’étenHue et la tononranhie de la rouneur oculaire sont analysés :
- • en nanne d’asnect hémorranique : hémorranie sous-conjonctivale. Fréquente, banale, habituellement unilatérale, indolore ou n’induisant qu’une sensation de tension locale lorsqu’elle est conséquente (patient sous anticoagulants par exemple), elle se présente sous la forme d’une tache hématique de couleur variant selon l’énaisseur du dénôt (fig. 6.2, e-fig. 6.3, fig. 6.4). Elle régresse en quelques semaines sans traitement mais doit faire rechercher une anomalie vasculaire locale ou une hypertension artérielle méconnue. Dans un contexte traumatique, une plaie de la conjonctive et du globe oculaire doit être systématiquement recherchée (fig. 6.5, e-fig. 6.6 à e-fig. 6.8). Au moindre doute, un scanner orbitaire sera demandé à la recherche d’un CEIO passé inaperçu. L’IRM est contre-indiquée tant que l’hypothèse d’un corns étranger métallique n’est pas formellement écartée;

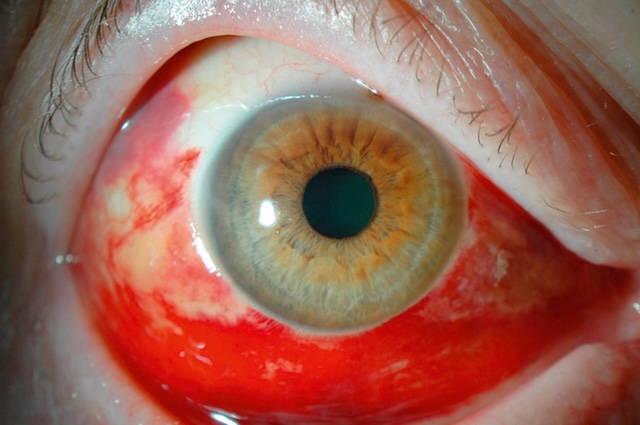
Fig. 6.2 Hémorragie sous-conjonctivale spontanée en flaque. On est ici face à une hémorragie sous-conjonctivale en nappe, spontanée, qui s’étale largement dans le quadrant inférieur de l’œil. La rougeur vive s’impose de façon très nette sous la conjonctive, sans débord vers la cornée ni signes d’irritation apparente. Le reste de l’œil est calme : la cornée est claire, la chambre antérieure bien formée, et la pupille reste centrée et réactive. C’est typiquement le genre d’hémorragie qui impressionne plus qu’elle n’alerte, souvent causée par un simple effort, une toux ou une pression brusque. Il n’y a aucun signe ici qui évoque une atteinte plus profonde. C’est le genre de situation qui ne nécessite pas d’intervention, juste une surveillance et un peu de repos.

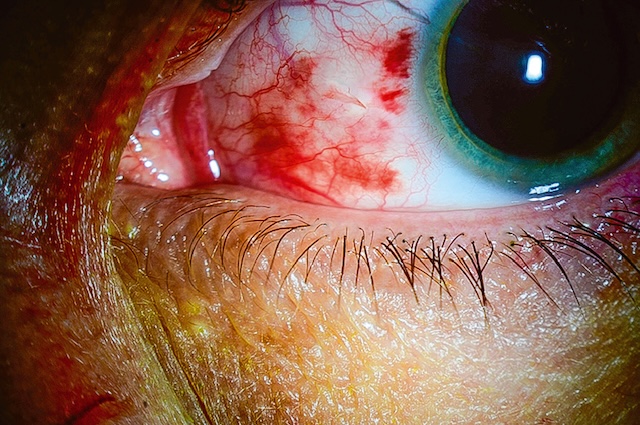
Fig. 6.4 œil rouge traumatique avec porte d’entrée d’un corps étranger intraoculaire postérieur. L’image présente un gros plan d’un œil traumatisé, visiblement injecté de sang avec une hyperhémie conjonctivale marquée, traduisant un œil rouge traumatique. À y regarder de plus près, on distingue une zone suspecte correspondant à une porte d’entrée, probablement perforante, par laquelle un corps étranger a pu pénétrer dans le globe oculaire. L’aspect de la cornée et les signes périphériques orientent vers une suspicion de présence intraoculaire postérieure, ce qui évoque une situation d’urgence ophtalmologique. Ce type de cliché clinique est typique d’un traumatisme oculaire grave nécessitant une prise en charge chirurgicale rapide et précise.

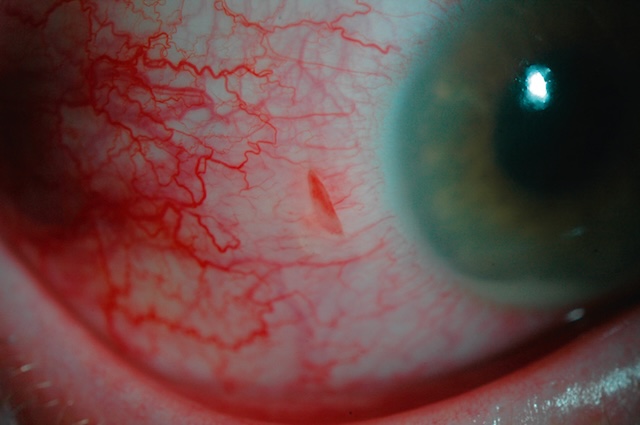
Fig. 6.5 Plaie de globe créée par la pénétration intraoculaire d’un corps étranger et compliquée d’une endophtalmie (hypopion). Ce gros plan clinique de l’œil révèle une lésion oculaire antérieure traumatique, clairement identifiable par la petite plaie linéaire visible dans la sclère à proximité du limbe cornéen. La conjonctive est fortement injectée, avec une hyperhémie diffuse et marquée de vaisseaux superficiels et profonds. Le point d’impact, souligné par une forme en fuseau rouge sombre, correspond à la zone de pénétration d’un corps étranger ayant traversé la paroi du globe. À l’intérieur de la chambre antérieure, la présence d’un hypopion traduit une réponse inflammatoire intense, typique d’une endophtalmie, complication infectieuse grave. L’aspect visuel global et la sévérité de la réaction soulignent une urgence ophtalmologique nécessitant une prise en charge rapide.
- • diffuse et sunerficielle : conjonctivite;
- • en secteur : énisclérite et sclérite;
- • autour du limbe sclérocornéen : vasodilatation concentrique des vaisseaux conjonctivaux limbiques, péricornéens sur 360° = cercle périkératique (fig. 6.9) : kératite ainuë; vaso-gilatation plus nrofonde = injection ciliaire : uvéite antérieure (fig. 6.10); vasodilatation sunerficielle pressionnelle = en tête de méduse : fistule artérioveineuse (fig. 6.11).

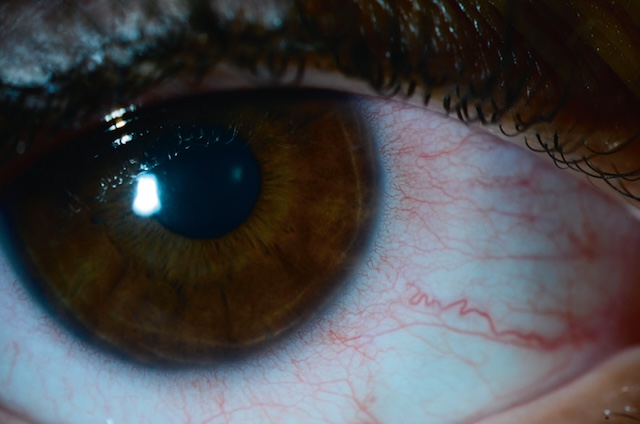
Fig. 6.9 Cercle périkératique. Ce cliché clinique illustre de manière frappante un cercle périkératique, parfaitement visible autour de la cornée. On observe une injection en anneau des vaisseaux ciliaires, qui forme une couronne rougeâtre dense au limbe, traduisant une irritation intraoculaire profonde. Cette hyperhémie périkératique est un signe caractéristique d’une inflammation de la chambre antérieure de l’œil, souvent associée à des affections telles que l’uvéite, la kératite ou un glaucome aigu. Le contraste entre la sclère plus blanche et la zone congestionnée rend le signe d’autant plus distinct, renforcé par la netteté de l’image capturée sous lumière focalisée.

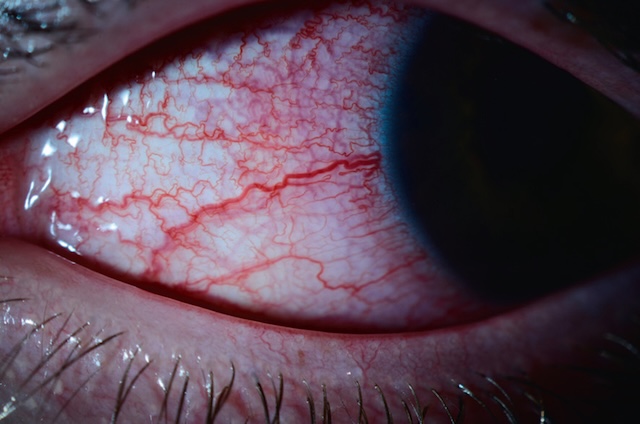
Fig. 6.10 Injection ciliaire profonde. Cette photographie ophtalmologique prise à travers un fond d’œil très agrandi met en évidence la présence d’un corps étranger métallique fiché profondément dans la rétine postérieure. L’objet est clairement identifiable par son éclat lumineux focalisé au centre de la rétine, contrastant avec les zones avoisinantes plus sombres. L’image est volontairement centrée et amplifiée pour révéler les reflets métalliques subtils ainsi que l’ombre en cône projetée par le fragment. La qualité légèrement floue en périphérie renforce l’effet de profondeur et signale un examen en lumière focalisée, typique de l’imagerie en lampe à fente avec lentille de condensation. Ce genre de lésion est souvent la conséquence d’un traumatisme pénétrant oculaire, nécessitant une prise en charge chirurgicale rapide afin de préserver au mieux la structure rétinienne et la fonction visuelle. On perçoit également les contours internes du globe oculaire ainsi que des modifications légères de la coloration rétinienne autour du point d’impact, pouvant évoquer un œdème réactionnel localisé ou un saignement discret.

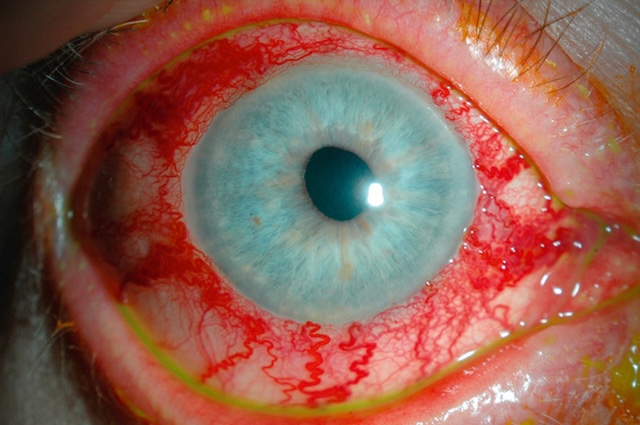
Fig. 6.11 Dilatation vasculaire en tête de méduse. Ce cliché ophtalmologique met en évidence un œil au bleu translucide contrastant vivement avec une congestion conjonctivale extrêmement marquée. Les vaisseaux dilatés et tortueux s'étendent de manière radiaire autour de la cornée, dessinant un motif en « tête de méduse » saisissant. Cette disposition vasculaire évoque une stase veineuse brutale, typique d’un phénomène de fistule artérioveineuse au niveau orbitaire, comme une fistule carotido-caverneuse. L’intensité de la rougeur, le calibre inhabituel des vaisseaux et leur disposition rayonnante suggèrent une hypertension veineuse locale significative. L’exsudation verdâtre au niveau du canthus inférieur laisse supposer l’instillation récente d’un collyre diagnostique. Ce type d’apparition vasculaire en toile d’araignée est non seulement caractéristique, mais il alerte immédiatement sur une pathologie sous-jacente potentiellement grave, souvent d’origine traumatique ou vasculaire.
3 114115Cornée
- • apprécier sa transparence : perte de transparence avec aspect grisâtre (œdème) ou blanchâtre (abcès, infiltrat inflammatoire stérile);
- • analyser sa sensibilité en la touchant délicatement avec un élément stérile souple et mousse;
- • repérer la présence d’un corps étranger à sa surface (fig. 6.12, e-fig. 6.13);

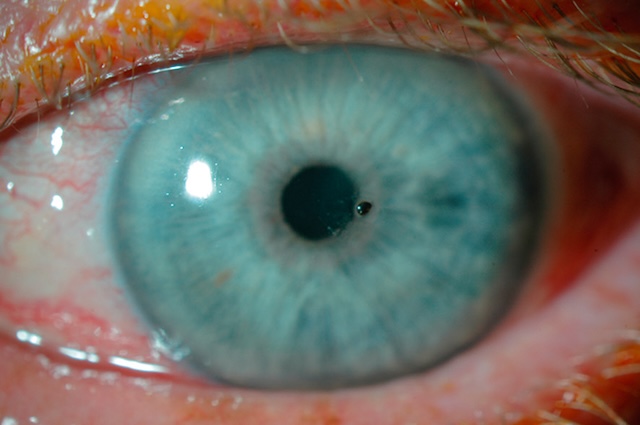
Fig. 6.12 Corps étranger cornéen superficiel métallique. Sur cette photo clinique d’une grande précision, on distingue parfaitement un œil à l’iris bleu clair, dans lequel un minuscule corps étranger métallique est incrusté en surface de la cornée, juste au niveau de l’axe visuel. Le petit point noir, bien centré, capte l’attention immédiatement. Il se détache sur la transparence naturelle de la cornée, indiquant qu’il s’agit d’un fragment métallique superficiel, probablement projeté lors d’un travail manuel sans protection oculaire. La clarté de l’image laisse également percevoir une discrète hyperémie conjonctivale dans les quadrants inférieurs, ce qui suggère une réaction inflammatoire locale débutante. L’œil semble par ailleurs bien hydraté, avec un film lacrymal uniforme sur la cornée. Ce type de situation nécessite une prise en charge rapide pour éviter la rouille cornéenne ou une kératite secondaire. C’est une photographie typique prise en lampe à fente, utilisée pour documenter l’emplacement exact avant extraction.
- • rechercher la présence de dépôts sur sa face postérieure : dépôts rétrocornéens (aussi appelés rétrodescemétiques) au cours des uvéites ou de certaines kératites stromales.
4 116Examen de la conjonctive palpébrale
- • des follicules (conjonctivite infectieuse virale ou bactérienne, fig. 6.14 e-fig. 6.15), des papilles (conjonctivite allergique de type printanière, fig. 6.16, e-fig. 6.17) ou une fibrose conjonctivale séquellaire;


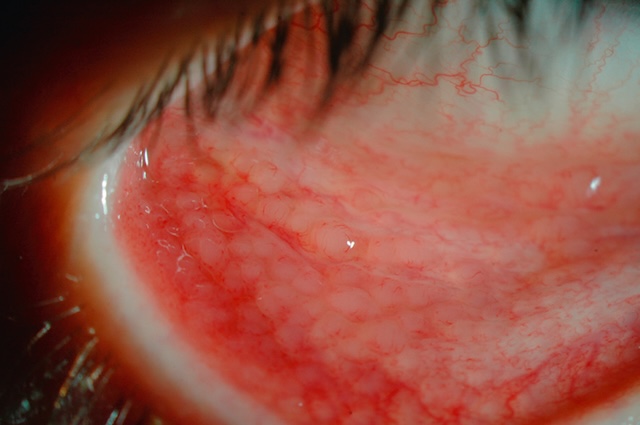
Fig. 6.14 Conjonctivite folliculaire inférieure.
Présence de follicules (hyperplasies lymphoïdes de la conjonctive cernées par des vaisseaux).Ce gros plan d’un examen clinique met en lumière une conjonctivite folliculaire localisée à la conjonctive palpébrale inférieure. La surface interne de la paupière est tapissée de multiples petites élévations arrondies et translucides, bien visibles, qui correspondent aux follicules lymphoïdes typiques d’une réaction inflammatoire chronique, souvent liée à une origine virale ou à une réaction à un collyre. La rougeur diffuse autour des follicules, ainsi que l’injection vasculaire, traduit une irritation conjonctivale importante. Le cliché, pris sous éclairage focal, permet d’observer en détail la texture irrégulière de la muqueuse palpébrale.

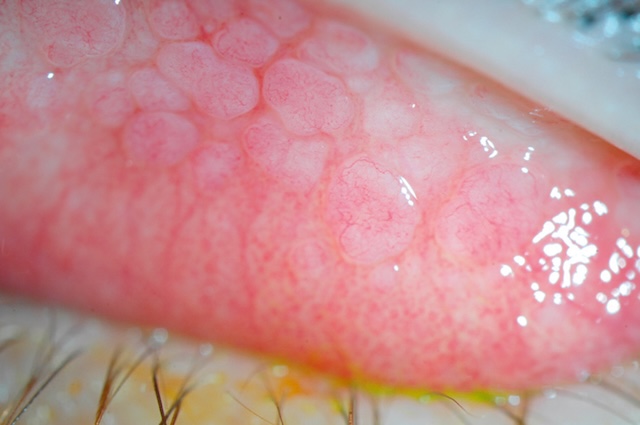
Fig. 6.16 Volumineuses papilles sur la conjonctive palpébrale supérieure (surélévations pédiculées de la conjonctive centrées par un vaisseau). Ce cliché clinique, d’une netteté impressionnante, présente un gros plan du versant interne de la paupière supérieure, précisément au niveau de la conjonctive palpébrale. On y distingue une multitude de papilles volumineuses, en relief net, à la surface rougeâtre et humide. Chaque papille est surélevée et structurée autour d’un fin vaisseau central, ce qui lui confère cet aspect pédiculé si caractéristique des réactions inflammatoires oculaires chroniques. L’image traduit visuellement ce que ressent le patient : inconfort, irritation, sensation de grain de sable. Cette configuration est typique d’une conjonctivite papillaire, souvent observée chez les porteurs de lentilles ou dans un contexte d’allergie sévère, marquée par un frottement mécanique répété. L’environnement conjonctival apparaît congestionné, révélant une hypervascularisation locale et une surproduction de mucus. C’est une photographie médicale puissante dans son réalisme, capturant la réponse tissulaire de l’œil à une agression prolongée.
- • un corps étranger sous la paupière supérieure en retournant la paupière de manière systématique pour s’exposer la conjonctive tarsale.

5 Examen de la surface oculaire après instillation d’un collyre à la fluorescéine (colorant orange) dans le cul-de-sac conjonctival
L’examen recherche des altérations de l’épithélium cornéen (abrasion ou ulcération) lors de l’éclairage avec une lumière bleue. L’addition d’un filtre jaune facilite encore leur mise en évidence. L’épithélium cornéen normal ne retient pas la fluorescéine qui, en revanche, se fixe sur le stroma dans les zones où l’épithélium est lésé ou défectueux; les altérations apparaissent vertes en lumière bleue. Leur aspect, leur nombre et leur localisation orientent le diagnostic :
- • une ulcération cornéenne unique et régulière évoque un traumatisme (fig. 6.18);

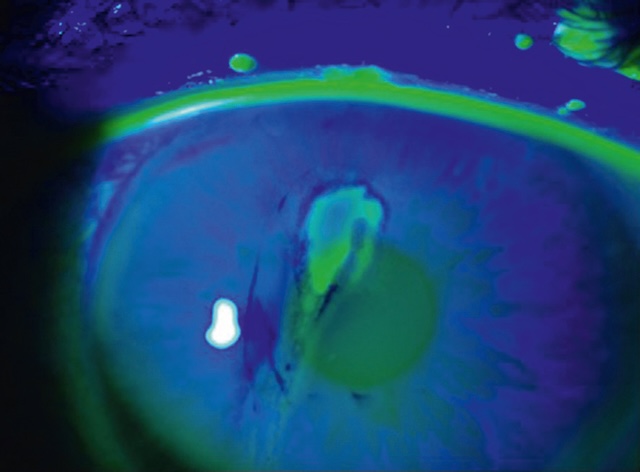
Fig. 6.18 Ulcération traumatique par allumette avec fluorescéine en lumière bleue. Sur cette vue en lumière bleue avec fluorescéine, on observe nettement une ulcération cornéenne centrale et verticale, avec des bords irréguliers et une zone d’imprégnation marquée, fluorescente en vert vif. Lésions compatibles avec un traumatisme par allumette, l’abrasion suit une trajectoire qui évoque un impact linéaire provoqué par un objet fin et allongé. Les contours de l’ulcération captent intensément la fluorescéine, signe d’une atteinte de l’épithélium cornéen. Une tache blanche isolée sur la périphérie évoque soit un second point d’impact soit une lésion associée. Le reste de la cornée présente des zones plus diffuses d’imprégnation, probablement dues à des micro-rayures ou des frottements secondaires. L’examen met en évidence une atteinte douloureuse et potentiellement à risque d’infection, nécessitant une prise en charge rapide.
- • une ulcération localisée avec une zone blanche adjacente évoque une kératite infectieuse bactérienne ou fongique avec un abcès de cornée, mais peut parfois aussi correspondre à une infiltration inflammatoire stérile;
- • un ulcère dendritique évoque une kératite herpétique;
- • 117de petites altérations épithéliales disséminées (kératite ponctuée superficielle [KPS]) évoquent en premier lieu un syndrome sec oculaire ou, dans un contexte aigu, les lésions cornéennes initiales d’une kératoconjonctivite à adénovirus;
- • des lésions linéaires (fig. 6.19) font rechercher un petit corps étranger passé inaperçu sous la paupière supérieure qui devra être retiré.

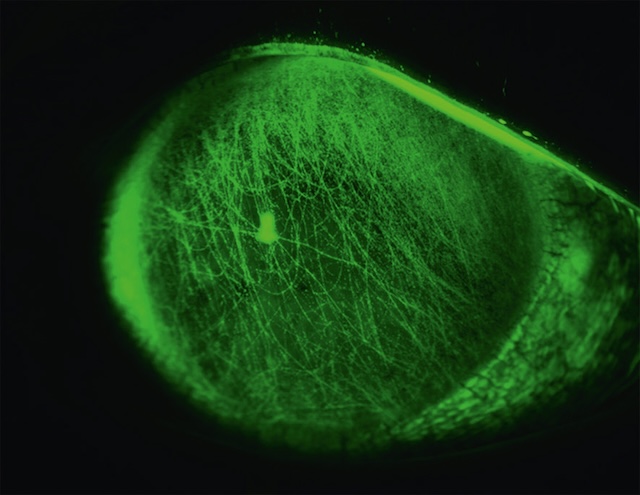
Fig. 6.19 Éraillures cornéennes linéaires par corps étranger sous-palpébral supérieur avec fluores-céine en lumière bleue et filtre jaune. Ce cliché biomédical en lumière bleue avec instillation de fluorescéine met en évidence des stries fluorescentes sur la surface cornéenne, orientées de façon verticale, caractéristiques d’éraillures linéaires. Ces lésions superficielles sont provoquées par un frottement répété d’un corps étranger coincé sous la paupière supérieure, tel qu’un grain de sable ou un cil. La zone la plus brillante, près du centre, suggère une lésion plus marquée ou un point de contact principal. La diffusion régulière de la fluorescéine sur le film lacrymal permet ici une lecture très précise de l’état de l’épithélium cornéen, essentiel pour identifier ce type d’abrasion traumatique.
Dans ces situations, chez un patient algique, photophobe et larmoyant, l’addition ponctuelle d’une goutte de collyre anesthésique pour le temps de l’examen facilitera grandement l’observation clinique.
6 Examen de la chambre antérieure
- • d’en apprécier la profondeur. Une chambre antérieure étroite ou plate plaide pour un glaucome aigu ou une hypotonie par plaie perforante, et une chambre antérieure trop profonde pour un recul du bloc ciliocristallinien avec déchirure de l’angle;
- • de rechercher à la lampe à fente les signes inflammatoires de l’uvéite antérieure (précipités rétrocornéens, effet Tyndall, hypopion – fig. 6.20, e-fig. 6.21 – membrane cyclitique ou bouchon de fibrine).

Fig. 6.20 Tyndall protéique (phare dans le brouillard) au cours d’une uvéite antérieure chronique protéique. Ce cliché en biomicrocopie, capturé à travers une lampe à fente, met en évidence un faisceau lumineux traversant la chambre antérieure de l’œil, révélant un phénomène de Tyndall protéique, typiquement comparé à un phare perçant dans un brouillard dense. Ce signal visuel subtil, mais significatif, trahit la présence de protéines en suspension dans l’humeur aqueuse, signe classique d’une uvéite antérieure chronique. L’environnement sombre renforce le contraste entre le faisceau lumineux et le liquide trouble qu’il traverse. Le reflet vertical très net de la lumière, doublé d’un léger flou diffus autour de ce faisceau, confirme la dispersion anormale des protéines et traduit l’activité inflammatoire intraoculaire. L’œil fixe en arrière-plan, avec sa pupille en arrière-plan floue, reste témoin silencieux de ce déséquilibre immunitaire persistant, révélateur de pathologies souvent auto-immunes ou infectieuses.
7 118Examen de l’iris et de la pupille
- • la présence de synéchies iridocristalliniennes, qui marque l’uvéite ou l’antécédent d’uvéite;
- • une atrophie irienne sectorielle en faveur d’une origine herpétique ou traumatique;
- • un myosis relatif, souvent présent dans l’uvéite antérieure aiguë et même parfois dans la kératite sévère;
- • une semi-mydriase aréflectique, fréquente au cours du glaucome aigu par fermeture de l’angle.
8 Mesure de la pression intraoculaire
Cette mesure est effectuée au tonomètre à air ou à aplanation, ou simplement estimée par un palper bidigital transpalpébral en l’absence d’instrument de mesure.
Une hypertonie évoque une crise aiguë de fermeture de l’angle, une crise néovasculaire ou une uvéite hypertensive.
Une hypotonie fait craindre une plaie oculaire transfixiante et il faut dans ce cas rechercher un signe de Seidel, c’est-à-dire une fuite d’humeur aqueuse qui va laver le film de fluorescéine.
9 Examen du fond d’œil
Après dilatation pupillaire par le tropicamide, l’examen du fond d’œil sera pratiqué devant toute pathologie pouvant s’accompagner d’une atteinte vitréenne ou rétinienne. Ainsi, la recherche d’une uvéite postérieure doit être systématique dès lors qu’il existe un tableau d’uvéite antérieure.
III Approche diagnostique et thérapeutique des infections et inflammations oculaires
L’approche diagnostique générale devant un œil rouge (sans l’usage spécialisé d’une lampe à fente) est schématisée dans la figure 6.22.

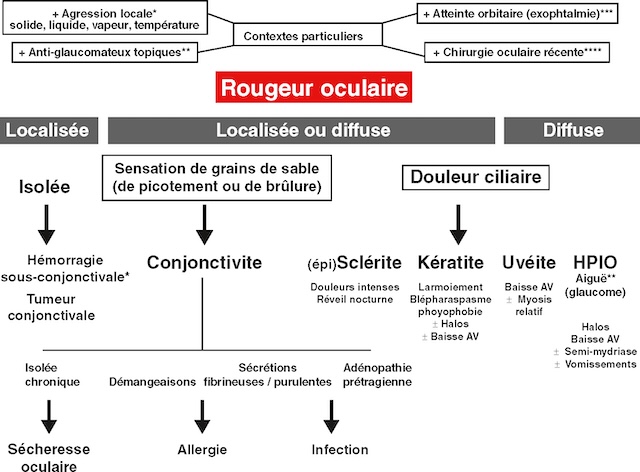
* Voir chapitre 11; ** voir chapitres 14, 16, 17, 20; *** voir chapitre 21; **** voir chapitres 10, 13, 14. AV : acuité visuelle; HPIO : hyperpression intraoculaire.
Ce schéma illustre de façon claire et pratique la démarche à adopter lorsqu’on est face à un patient présentant une rougeur oculaire. D’un coup d'œil, on comprend comment orienter la recherche étiologique en fonction de la localisation de la rougeur : localisée, localisée ou diffuse, ou bien diffuse. Lorsqu’elle est isolée et bien délimitée, une simple hémorragie sous-conjonctivale ou une sécheresse oculaire chronique peut être en cause. Si le patient parle d’une sensation de sable ou de brûlure dans l’œil, on s’oriente vers une conjonctivite, une allergie ou une infection selon l’aspect des sécrétions et les signes associés. Les douleurs plus profondes, dites ciliaires, sont à prendre au sérieux car elles peuvent révéler une kératite, une uvéite ou une crise aiguë de glaucome (HPIO), surtout si la vision baisse ou que des halos apparaissent. Le schéma tient compte aussi de certains contextes particuliers comme la prise de collyres, une chirurgie récente ou des signes orbitaires. L’ensemble est construit pour que l’œil clinicien ne perde pas de temps et puisse poser les bonnes questions avec méthode et efficacité.
Après avoir recherché les éléments contextuels importants (notion de traumatisme physique, chimique ou thermique récent, d’antécédent de chirurgie, d’anomalies orbitaires ou palpé-brales, de traitements locaux en cours) pour extraire ces situations particulières de la démarche 119generale, l’orientation se fait ensuite en fonction de la localisation et de l’aspect de la rougeur oculaire, et se fonde également sur l’existence de signes associes qui peuvent parfois être au premier plan du tableau clinique et sont évocateurs de certains diagnostics.
Ainsi, le constat d’un œil rouge sans baisse d’acuité visuelle est habituellement le fruit d’une atteinte pariétale ne touchant pas l’axe optique cornéen, tandis que la survenue d’une baisse d’acuité visuelle sur un œil infecté ou inflammatoire provient d’un trouble des milieux sur l’axe visuel ou d’une lésion rétinienne centrale. Si une lampe à fente est disponible, l’examen amène des éléments supplémentaires au diagnostic, notamment en cas de kératite (analyse de l’atteinte dans l’épaisseur cornéenne), d’uvéite (présence d’un effet Tyndall et de précipités rétrocornéens) ou de glaucome aigu à angle fermé (mise en évidence d’un œdème cornéen, présence d’une chambre antérieure étroite et d’un angle iridocornéen fermé).
A Conjonctivites
Les affections de la conjonctive ont un cortège de signes communs qui témoignent d’une irritation de surface et sont souvent décrits comme plus gênants que douloureux. De ce fait, les patients atteints de conjonctivite rapportent une sensation de corps étranger, de grains de sable ou de poussière, parfois par un prurit, une perception de brûlure ou de cuisson. Fréquentes, uni- ou bilatérales (fig. 6.23, e-fig. 6.24, e-fig. 6.25 ), les conjonctivites sont d’origines variées, qu’elles soient de causes infectieuses, inflammatoires ou encore allergiques.
), les conjonctivites sont d’origines variées, qu’elles soient de causes infectieuses, inflammatoires ou encore allergiques.

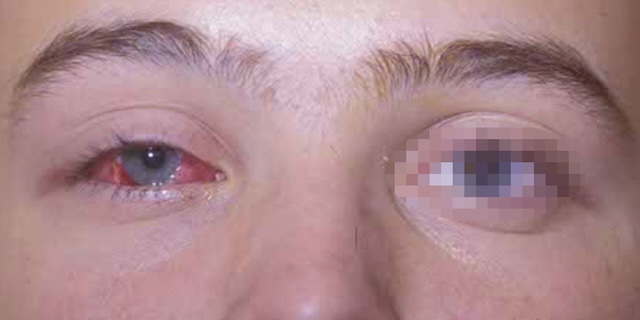
L’œil droit de ce jeune patient présente une rougeur marquée, particulièrement au niveau de la conjonctive bulbaire, signe typique d’un épisode de conjonctivite. L’hyperhémie conjonctivale est bien localisée, asymétrique, avec une absence d’atteinte à l’œil gauche, qui reste calme et sans injection. L’absence d’œdème palpébral ou de sécrétions visibles suggère une forme modérée, probablement d’origine virale ou irritative. La sclère reste visible malgré la rougeur, ce qui exclut une hémorragie sous-conjonctivale. La paupière n’est pas franchement tuméfiée, mais l’œil paraît légèrement fatigué, traduisant un inconfort ressenti par le patient. L’aspect unilatéral doit faire penser à une cause infectieuse locale ou à un contact allergène d’un seul côté.
La présence de sécrétions devant l’axe optique entraîne une gêne visuelle transitoire améliorée par le clignement palpébral ou le lavage. La survenue d’une baisse d’acuité visuelle permanente et de douleurs témoigne d’une atteinte cornéenne centrale et donc d’une kératoconjonctivite.
1 120Conjonctivites bactériennes aiguës
Ces conjonctivites se présentent sous la forme d’une rougeur conjonctivale diffuse, prédominant dans le cul-de-sac inférieur, peuvent être uni-ou bilatérales, parfois avec un intervalle libre avant l’atteinte du deuxième œil.
La rougeur s’accompagne de sécrétions mucopurulentes (fig. 6.26) collant les paupières le matin au réveil avec un aspect en poils de pinceau, et volontiers d’un chémosis et d’un œdème palpébral dans les cas plus sévères. Bien que les germes en cause varient en fonction de l’âge et du terrain, les conjonctivites bactériennes aiguës sont dues le plus souvent à des cocci à Gram positif (principalement streptocoque ou staphylocoque), et guérissent habituellement sans séquelles. Un trouble de perméabilité des voies lacrymales doit être secondairement recherché, notamment aux âges extrêmes de la vie, en cas de larmoiement chronique ou d’épisodes infectieux récurrents.

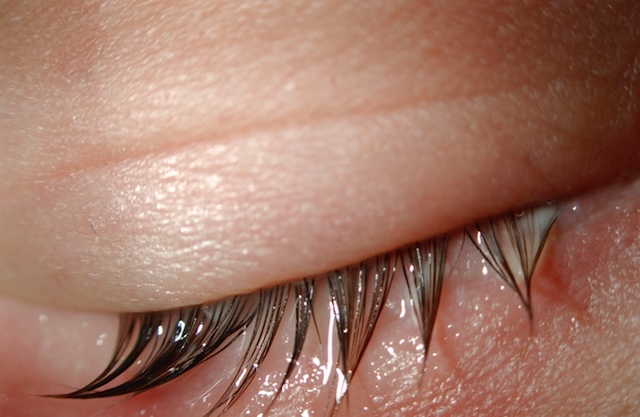
Présence de sécrétions purulentes avec cils en poils de pinceau.
Ce gros plan photographique montre un œil fermé dont les cils sont visiblement collés entre eux par un écoulement séreux ou purulent, évocateur d’une conjonctivite bactérienne. Ce type d’image appartient au registre de l’observation clinique en ophtalmologie. Les sécrétions épaisses présentes à la base des cils, à la jonction palpébrale, signalent une prolifération microbienne, souvent à germes gram positifs. La paupière inférieure semble légèrement enflammée, avec un aspect humide et luisant du bord libre, typique d’une réponse inflammatoire conjonctivale. L’absence d’hyperhémie marquée à ce stade suggère une phase modérée, mais l’agglutination des cils au réveil est un signe fréquent rapporté dans les formes bactériennes. L’image illustre de manière simple mais éloquente une affection oculaire fréquente, soulignant l’importance de l’examen minutieux des annexes de l’œil en consultation.
Le traitement probabiliste sans prélèvement de première intention comprend :
- • hygiène des mains : prévention vis-à-vis de l’entourage;
- • lavages des sécrétions au sérum physiologique ou avec un soluté isotonique pharmaceutique;
- • collyre antiseptique 4 à 6 fois/jour qui s’avère habituellement suffisant. L’antibiothérapie n’est donc pas systématique en l’absence de signe de gravité. Dans le cas contraire, elle sera prescrite avec la même fréquence et ciblée sur les cocci à Gram positif.
![]() Devant une forme grave ou résistante à ce traitement de première ligne, un prélèvement conjonctival par écouvillonnage est effectué et transféré au laboratoire dans un milieu de transport adapté pour être mis en culture.
Devant une forme grave ou résistante à ce traitement de première ligne, un prélèvement conjonctival par écouvillonnage est effectué et transféré au laboratoire dans un milieu de transport adapté pour être mis en culture. ![]() Un antibiogramme ou un antifongigramme permettra d’adapter le traitement aux résultat obtenus.
Un antibiogramme ou un antifongigramme permettra d’adapter le traitement aux résultat obtenus.
2 121Conjonctivites bactériennes chroniques : conjonctivites à Chlamydia
Certaines conjonctivites bactériennes évoluent sur un mode chronique, induisant en règle l’apparition d’une adénopathie prétragienne. C’est le cas notamment des infections à Chlamydia (fig. 6.27), mais aussi à Bartonnella henselae ou exceptionnellement à mycobacté-ries. ![]() Le prélèvement conjonctival sert alors à la recherche diagnostique moléculaire par PCR du pathogène suspecté.
Le prélèvement conjonctival sert alors à la recherche diagnostique moléculaire par PCR du pathogène suspecté.

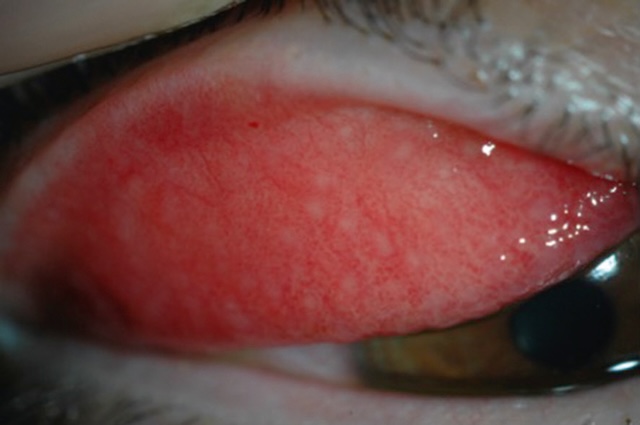
Sur cette photographie en très gros plan de la paupière supérieure eversée, l’on distingue nettement l’aspect typique d’une conjonctivite folliculaire. La muqueuse conjonctivale est rouge vif, parsemée de multiples follicules bien arrondis, légèrement surélevés, évoquant une inflammation persistante. Le regard se porte vers l’arcade tarsale, où la texture bosselée est particulièrement caractéristique d’une infection à Chlamydia. Cette image traduit visuellement l’agression chronique de la surface oculaire par cet agent pathogène, souvent silencieux au début mais redoutable lorsqu’il s’installe. La cornée, en partie visible, semble intacte, ce qui oriente vers une atteinte limitée à la conjonctive à ce stade. L’aspect clinique global renforce l'importance de l’observation minutieuse de l’intérieur des paupières dans toute suspicion de conjonctivite persistante ou récidivante.
![]() Le trachome (conjonctivite à Chlamydia trachomatis) est très fréquent dans les pays les moins avancés et sévit majoritairement sur le continent africain. Il s’agit d’une conjonctivite bilatérale avec fibrose du tarse et entropion induisant une néovascularisation cornéenne. Sa prise en charge repose sur le traitement antibiotique de l’infection par azithromycine ou tétra-cyclines et la cure chirurgicale des complications palpébrales.
Le trachome (conjonctivite à Chlamydia trachomatis) est très fréquent dans les pays les moins avancés et sévit majoritairement sur le continent africain. Il s’agit d’une conjonctivite bilatérale avec fibrose du tarse et entropion induisant une néovascularisation cornéenne. Sa prise en charge repose sur le traitement antibiotique de l’infection par azithromycine ou tétra-cyclines et la cure chirurgicale des complications palpébrales.
La conjonctivite à inclusions de l’adulte est une affection sexuellement transmissible uni- ou bilatérale, qui peut s’associer à une urétrite ou une vaginite et sera donc généralement traitée par azithromycine orale en monodose.
3 Conjonctivites virales
Très fréquentes, extrêmement contagieuses, liées en premier lieu à certains sérotypes d’adéno-virus, les conjonctivites virales surviennent par épidémies et touchent plusieurs personnes au sein d’une famille ou d’une collectivité.
L’atteinte commence souvent d’un côté et se bilatéralise par autocontamination dans les jours qui suivent. Le tableau comporte :
- • une hyperhémie conjonctivale franche souvent accompagnée d’hémorragies et parfois de fausses membranes (fig. 6.28, fig. 6.29, e-fig. 6.30);

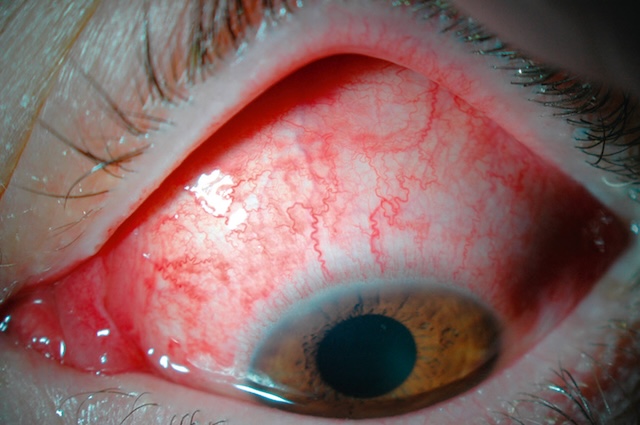
Fig. 6.28 Conjonctivite à adenovirus à composante hémorragique. Ce cliché montre un œil ouvert en grand, avec une injection conjonctivale très marquée. Les vaisseaux sont dilatés et sinueux, dessinant un réseau rouge vif qui serpente sur toute la conjonctive bulbaire, témoignant d’un processus inflammatoire aigu. À cela s’ajoute une composante hémorragique bien visible, sous forme de nappes rouges plus profondes, en particulier au niveau nasal et inférieur, indiquant de petites hémorragies sous-conjonctivales associées. L’iris brun noisette reste bien centré et la cornée claire, mais c’est surtout la souffrance de la conjonctive qui attire le regard, typique d’une conjonctivite virale due à un adénovirus, souvent très contagieuse. L’aspect œdémateux et les rougeurs marquées sont les signes d’un œil très irrité, probablement douloureux et larmoyant pour le patient.

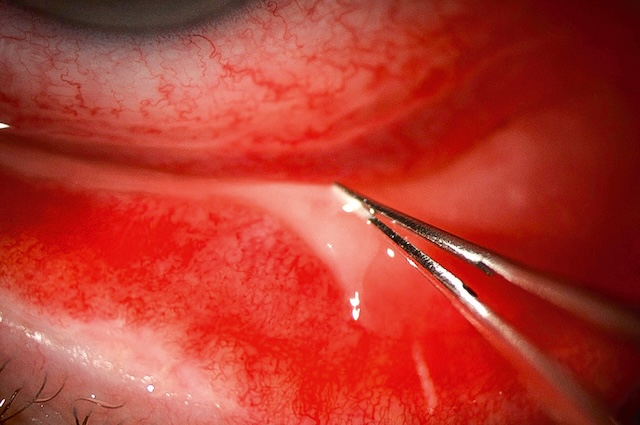
Fig. 6.29 Fausses membranes de conjonctivite adénovirale. Cette photographie en très gros plan d’un œil, prise en condition de biomicroscopie, montre une conjonctive palpébrale inférieure extrêmement inflammée, envahie par un réseau vasculaire dense et rouge vif, révélateur d’un processus aigu. L’image capte un moment clinique précis où une pince atraumatique retire délicatement une fausse membrane blanchâtre et semi-transparente, plaquée à la surface conjonctivale. Cette membrane pseudo-fibrineuse, adhérente mais amovible, est typique des formes sévères de conjonctivite adénovirale. L’intervention chirurgicale de retrait se fait sous contrôle visuel pour éviter d'endommager l’épithélium sous-jacent fragilisé. On ressent ici la précision du geste dans un contexte infectieux très actif.
- • des sécrétions claires;
- • une adénopathie prétragienne sensible à la palpation qui signe la cause infectieuse et conforte le diagnostic.
Dans leur phase folliculaire, elles sont parfois difficiles à distinguer d’une conjonctivite bactérienne. ![]() Si nécessaire, l’étiologie virale peut être confirmée par un test antigénique rapide sur un échantillon lacrymal conjonctival ou par un test PCR spécifique lorsqu’il est disponible.
Si nécessaire, l’étiologie virale peut être confirmée par un test antigénique rapide sur un échantillon lacrymal conjonctival ou par un test PCR spécifique lorsqu’il est disponible.
![]() L’évolution est en règle spontanément favorable en 10 à 15 jours, mais la conjonctivite virale peut se compliquer de membranes fibrineuses dans les cas les plus graves et/ou évoluer vers un tableau de kératoconjonctivite (voir plus loin).
L’évolution est en règle spontanément favorable en 10 à 15 jours, mais la conjonctivite virale peut se compliquer de membranes fibrineuses dans les cas les plus graves et/ou évoluer vers un tableau de kératoconjonctivite (voir plus loin).
La prise en charge est essentiellement symptomatique, se limitant au nettoyage de la surface oculaire et à l’instillation de produits mouillants. Les corticoïdes locaux ne sont par ailleurs 122prescrits que dans les formes sévères après ablation des membranes car leur utilisation prolonge la durée du portage viral.
a Conjonctivite allergique saisonnière
Cette conjonctivite survient comme attendu de façon saisonnière à chaque fois que l’allergène en cause est rencontré, le plus souvent sur terrain atopique ou allergique connu.
Bilatérale et récidivante, la crise allergique se caractérise par l’existence d’un prurit et montre une conjonctive rosée, résultante du mélange d’un chémosis blanc laiteux et d’une dilatation des vaisseaux conjonctivaux (fig. 6.31). À cela s’ajoutent des sécrétions claires, une discrète hypertrophie papillaire de la conjonctive tarsale supérieure et un œdème palpébral modéré.

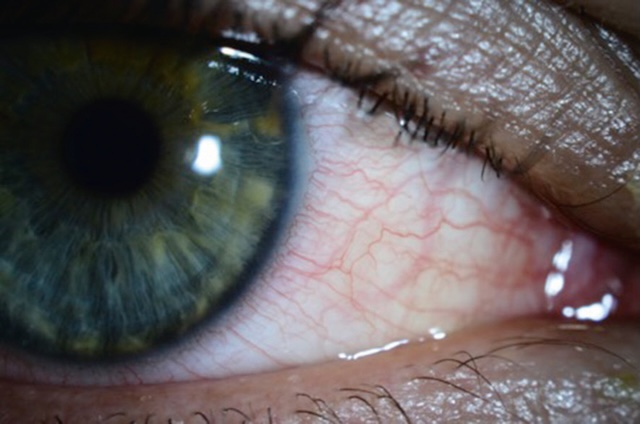
Ce cliché photographique en très gros plan capte avec précision l’œil d’un patient présentant une conjonctivite allergique saisonnière. L’aspect général du globe oculaire, bien que relativement calme, révèle un discret chémosis — cet œdème léger de la conjonctive visible sous la paupière inférieure, traduisant une inflammation d’origine allergique. Les vaisseaux conjonctivaux sont dilatés de façon modérée, enchevêtrés dans le blanc de l’œil, donnant cet aspect injecté typique mais sans rougeur excessive. La cornée reste parfaitement claire, sans sécrétions visibles, ce qui est compatible avec une forme non infectieuse. L’iris, bien défini, semble légèrement rétracté du fait de l’ouverture de l’œil en latéral, offrant une belle visualisation du bord ciliaire. L’image appartient clairement à la catégorie des photographies cliniques orientées vers l’étude des affections allergiques oculaires, souvent déclenchées par le pollen ou la poussière. Cette manifestation discrète, bien que bénigne, illustre toute la subtilité de l’examen ophtalmologique en période pollinique.
Après une enquête minutieuse, le bilan allergologique recherche le ou les allergènes en cause au moyen de tests épicutanés ou, plus exceptionnellement, de tests de provocation conjonctivale.
- • des lavages conjonctivaux avec un soluté isotonique;
- • l’instillation d’un collyre anti-allergique (antihistaminique, antidégranulant mastocytaire) ou parfois d’un corticoïde en cure courte si les manifestations sont intenses;
- • une éviction de l’allergène, voire une désensibilisation lorsqu’elle est possible et nécessaire.
c Kératoconjonctivite vernale (ou conjonctivite printanière)
Cette forme grave d’allergie oculaire chronique pédiatrique touche principalement les garçons avant la puberté. Les lésions conjonctivales de fond s’acutisent en période chaude et ensoleillée le printemps ou l’été, entraînant alors un prurit intense, puis avec l’apparition de l’atteinte cornéenne s’ajoutent une photophobie, un blépharospasme et un larmoiement fréquemment invalidants.
Deux types de présentation sont possibles et parfois associés :
- • la forme limbique prend l’aspect d’un bourrelet rosé périkératique souvent associé à des infiltrats blanchâtres ponctiformes appelés grains de Trantas (fig. 6.32);

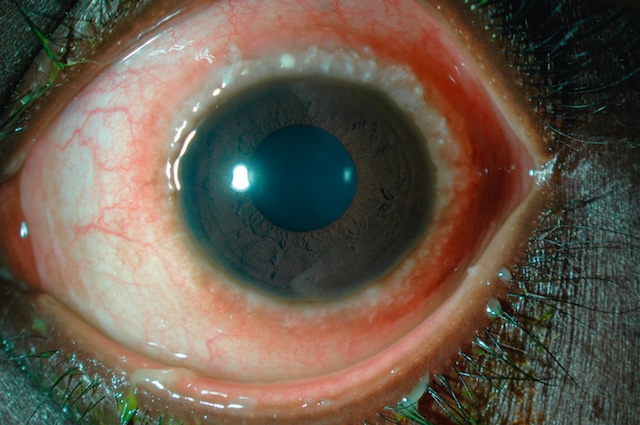
Fig. 6.32 Bourrelet limbique avec grains de Trantas et sécrétions fibrineuses. L’œil capturé dans cette vue rapprochée révèle avec précision une conjonctive limbique supérieure nettement épaissie, formant un bourrelet blanchâtre, typique des réactions allergiques oculaires sévères. Ce bourrelet, adjacent à la cornée, est accompagné de multiples grains de Trantas, ces petits amas blancs éosinophiliques qui ponctuent le limbe, souvent retrouvés dans les conjonctivites allergiques chroniques comme la kératoconjonctivite vernale. La sclère périphérique est hyperhémique, témoignant d’une congestion conjonctivale active. On distingue aussi des sécrétions fibrineuses au niveau du sillon conjonctival inférieur, traduisant une inflammation en cours. L’ensemble dessine une réponse immunitaire marquée et localisée, illustrant parfaitement le tableau clinique d’une allergie oculaire avancée. L’examen de ce type nécessite une attention particulière pour évaluer le retentissement cornéen potentiel.
- • la forme tarsale est la plus grave car les lésions pavimenteuses ou papilles de la conjonctive palpébrale supérieure (fig. 6.33) agressent directement la cornée, provoquant en règle une kératite épithéliale ponctuée, parfois la survenue d’une ulcération épithéliale arrondie ou ovalaire (ulcération vernale, fig. 6.34) et plus rarement la constitution d’une plaque solide réactionnelle (plaque vernale). La présence de sécrétions fibrineuses ou muciniques est également possible.

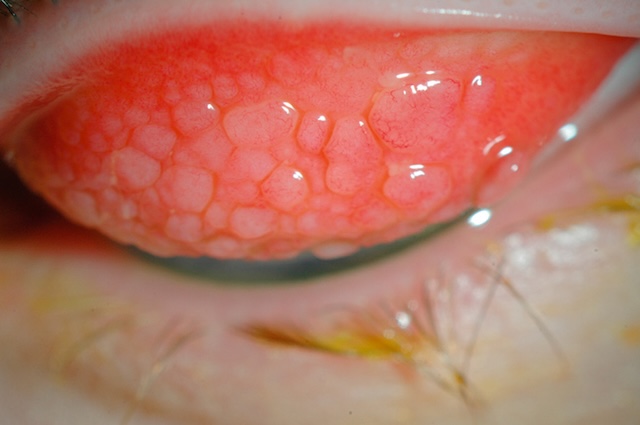
Fig. 6.33 Forme tarsale avec lésions pavimenteuses. Ce gros plan de la conjonctive tarsale supérieure met en évidence une inflammation prononcée caractérisée par de larges papilles surélevées et irrégulières. Ces lésions pavimenteuses, visibles sur toute la surface du tarse, apparaissent comme des structures translucides, arrondies, parfois confluentes, qui donnent un aspect granuleux typique. La teinte rouge vif du fond conjonctival traduit une hyperhémie importante, signe d’une réaction immunitaire active. La surface luisante et la présence d’un film lacrymal accentuent le relief des papilles, souvent observées dans des formes sévères de conjonctivites allergiques ou dans certaines kératoconjonctivites chroniques. L’irritation semble marquée, possiblement accompagnée de démangeaisons intenses ou d’un larmoiement constant.

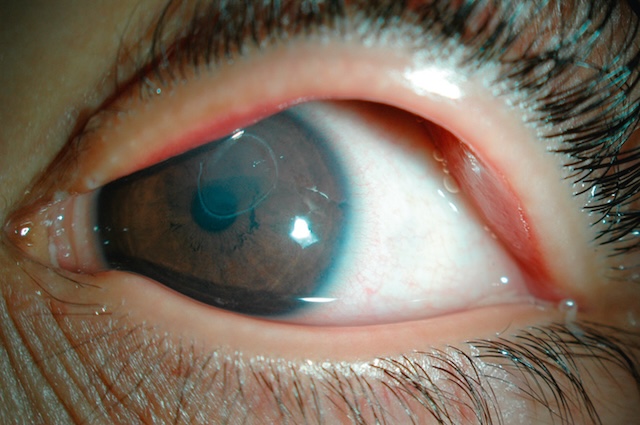
Fig. 6.34 Ulcération vernale arrondie d’aspect grisé entourée de son liseré épithélial. Cette photographie en haute résolution montre l’œil ouvert en grand, capturant la cornée dans son intégralité. On y observe distinctement une ulcération vernale de forme arrondie, au centre de la zone optique, caractérisée par une teinte grisée qui contraste subtilement avec la clarté naturelle de la cornée environnante. Cette lésion superficielle est délimitée par un fin liseré épithélial, typique de l’ulcère vernale, signe révélateur d’une kératoconjonctivite allergique chronique. Le regard figé vers le haut accentue la visibilité de cette atteinte cornéenne, suggérant une gêne persistante, notamment photophobie ou sensation de corps étranger. Le cliché met en lumière à la fois la localisation centrale de l’ulcère et la finesse de son contour, captant un instant clinique crucial pour le diagnostic et la prise en charge ophtalmologique.
Le traitement recourt spécifiquement à l’instillation de corticoïdes topiques en phase aiguë et/ou de ciclosporine en collyre pour le traitement de fond, en sus des éléments énoncés plus haut utilisés de manière usuelle.
d 124Kératoconjonctivite de la dermatite atopique
Manifestation oculaire chronique, fréquente et potentiellement sévère de la dermatite atopique, la kératoconjonctivite atopique atteint avec prédilection les hommes adultes. L’eczéma des paupières s’ajoute ici aux lésions allergiques conjonctivales et cornéennes qui ressemblent volontiers à celles de la kératoconjonctivite vernale. La survenue d’un ectropion par rigidité cutanée est fréquente (fig. 6.35) et dégrade encore les moyens de défense locale. De multiples complications oculaires sont possibles et doivent être recherchées : kératocône induit par la friction des paupières, infections conjonctivale et/ou cornéenne, cataracte spécifique en écus-son antérieur ou cortisonée sous-capsulaire postérieure, glaucome induit par les corticoïdes (voir chapitre 14).

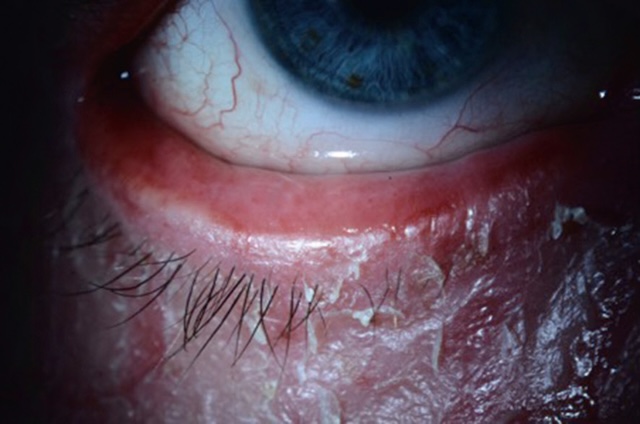
La photographie médicale présentée montre l’œil d’un patient vu de près, centré sur la paupière inférieure gauche, clairement éversée, ce qui expose largement la conjonctive inférieure. Cette éversion est typique d’un ectropion, qui dans ce cas semble d’origine inflammatoire. La peau entourant la paupière, notamment sur la joue, présente un aspect craquelé, sec, blanchâtre par endroits et rouge en d’autres zones, caractéristique d’un eczéma palpébral sévère. L’épiderme est visiblement irrité et desquamé, traduisant une inflammation chronique avec une perte d’élasticité cutanée. La conjonctive exposée apparaît rougeâtre et congestionnée, ce qui évoque une fibrose conjonctivale associée à l’inflammation prolongée. L’œil lui-même reste ouvert, révélant une cornée claire et un iris bleu, sans trouble apparent, ce qui met en évidence le contraste entre l’état du globe oculaire et celui des tissus périphériques. Ce cliché correspond à une situation clinique où la dermatite sévère entraîne une modification mécanique de la position de la paupière, altérant la protection oculaire normale.
125La prise en charge thérapeutique repose sur les corticoïdes et les immunosuppresseurs locaux, y compris ceux déposés sur le versant cutané eczémateux comme le tacrolimus, associés aux traitements anti-allergiques et mouillants usuels.
e Conjonctivite de l’allergie de contact
Dans ce cadre, l’atteinte oculaire comme l’atteinte palpébrale sont liées à une hypersensibilité non immédiate à un allergène de contact. Ce dernier est habituellement d’origine médicamenteuse (allergie aux collyres antibiotiques, mydriatiques ou antiglaucomateux notamment), cosmétique ou professionnelle et peut être appliqué directement sur le site oculopalpébral, être manuporté ou aéroporté. L’importance de l’eczéma palpébral de contact et l’interrogatoire orientent le diagnostic. La conjonctivite est assez peu spécifique et la réaction s’étend jusqu’au bord libre de la paupière.
Le traitement repose avant tout sur l’éviction de l’allergène tandis qu’une corticothérapie locale transitoire est prescrite en cas de réaction intense.
5 Kératoconjonctivite sèche ou sécheresse oculaire
Très fréquente, plus souvent qualitative que quantitative, l’insuffisance de la sécrétion lacrymale est la première étiologie de conjonctivite. Elle se présente donc sous la forme d’une rougeur oculaire habituellement modérée associée à une sensation de grains de sable ou à des douleurs oculaires superficielles. Ces signes sont secondaires à une atteinte de l’épithélium conjonctival, associée ou non à une atteinte épithéliale cornéenne, par altération de la trophicité des cellules épithéliales. Les syndromes secs sévères peuvent entraîner une baisse d’acuité visuelle par atteinte épithéliale cornéenne centrale ou simplement par rupture prolongée du film lacrymal altérant la qualité du dioptre cornéen.
- • un examen quantitatif de la sécrétion lacrymale : le test de Schirmer. Réalisé sans anesthé-sie, il consiste à placer une bandelette de papier graduée au niveau du cul-de-sac conjonc-tival inférieur et à mesurer la zone humidifiée après 5 minutes. L’hyposécrétion est franche si l’imprégnation est inférieure à 5 mm;
- • une estimation quantitative de la qualité du film lacrymal : le temps de rupture du film lacrymal ou break-up time (BUT). Après instillation d’une goutte de fluorescéine dans le cul-de-sac conjonctival inférieur, celle-ci se répartit dans le film lacrymal lors des clignements, permettant sa visualisation avec un filtre bleu. On peut alors analyser la stabilité du film lacrymal en demandant au patient de stopper tout clignement palpébral et en chronométrant le délai de rupture spontanée (fig. 6.36);

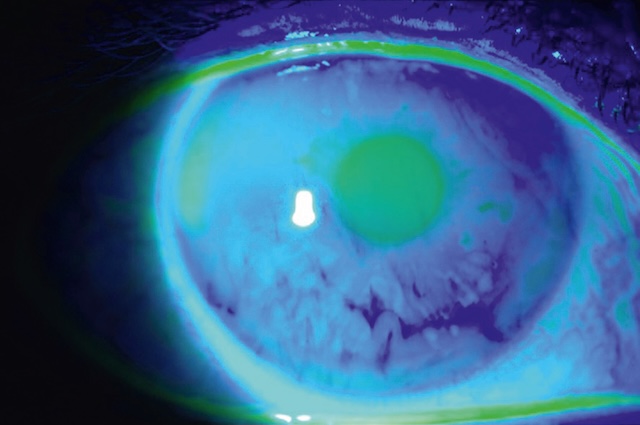
Fig. 6.36 Break-up time (BUT) : mesure du temps de rupture du film lacrymal après instillation d’une goutte de fluorescéine. Ce cliché en lumière bleue correspond à une photographie ophtalmologique réalisée lors d’un examen du film lacrymal par fluorescéine. L’œil observé a été instillé avec une goutte de colorant fluorescent, puis exposé à une lumière cobalt bleue afin d’évaluer le break-up time (BUT), c’est-à-dire le temps de rupture du film lacrymal. Sur cette image, la surface cornéenne apparaît teintée de bleu avec des zones plus sombres, particulièrement dans la région centrale, où la fluorescéine s’est répartie de manière irrégulière. Ces zones indiquent des altérations de stabilité du film lacrymal, suggérant une sécheresse oculaire. La limite du film sur le pourtour est bien marquée et le reflet lumineux au centre indique la clarté optique persistante de la cornée. Ce type d’image est utilisé en routine clinique pour objectiver un défaut de lubrification oculaire, souvent associé à un inconfort, une sensation de sable ou une irritation chronique chez le patient.
- • un examen de la surface cornéenne par instillation d’une goutte de fluorescéine qui montre la kératopathie épithéliale ponctuée à l’examen en lumière bleue, et plus encore si l’on s’aide d’un filtre jaune (fig. 6.37, e-fig. 6.38, e-fig. 6.39);

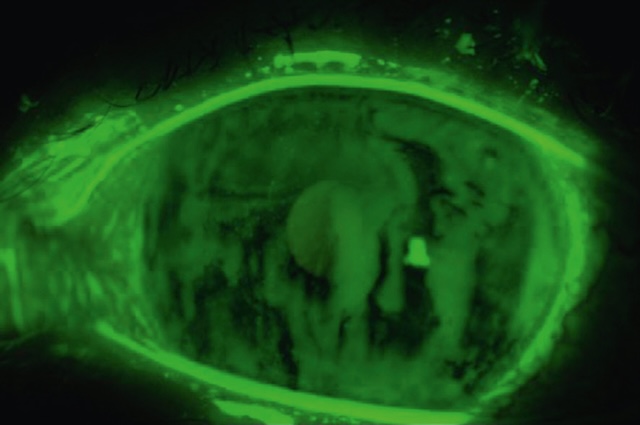
Fig. 6.37 Rupture du film lacrymal et fin marquage épithélial (fluorescéine + lumière bleue + filtre jaune). Photographie biomédicale obtenue par instillation de fluorescéine et observation sous lumière bleue à l’aide d’un filtre jaune, mettant en évidence une rupture nette et diffuse du film lacrymal. La surface cornéenne révèle un marquage épithélial important, caractérisé par des zones irrégulièrement imbibées de fluorescéine, traduisant une atteinte franche de l’épithélium. On distingue clairement des traînées verticales fluorescentes, signe d’un assèchement avancé et d’une instabilité lacrymale persistante. La cornée, partiellement éclairée, présente des plages de coloration intense, marquant les zones d'altération. Ce cliché illustre une sécheresse oculaire pathologique avec altération marquée de la surface oculaire.
- • un examen de la surface conjonctivale par la même technique de fluorescéine qui permet de grader la kératoconjonctivite sèche (classification d’Oxford) ou après application de vert de lissamine (peu utilisé en pratique clinique) qui colore les cellules épithéliales moribondes dans la zone d’ouverture palpébrale (fig. 6.40, e-fig. 6.41 à e-fig. 6.43).

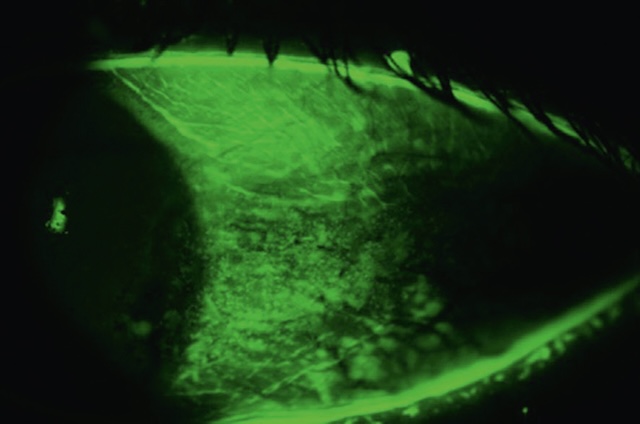
Fig. 6.40 Lésions de kératoconjonctivite sèche dans l’espace interpalpébral (fluorescéine + lumière bleue + filtre jaune).
Épisclérite nasale gauche.Dans cette photographie en lumière bleue avec filtre jaune, l’œil est observé après instillation de fluorescéine afin de mettre en évidence des lésions de kératoconjonctivite sèche. L’espace interpalpébral présente une distribution diffuse de colorations vertes révélant une atteinte marquée de la surface cornéenne. On distingue des zones de dessiccation épithéliale, en particulier sur la cornée inférieure, avec une texture irrégulière et granuleuse. Les arborisations de décoloration indiquent une perte de cellules épithéliales, tandis que la limite supérieure de l’image montre une ligne fluorescente soulignant le bord tarsal. L’ensemble de l’image met en lumière une atteinte chronique de la surface oculaire, typique d’un syndrome sec modéré à sévère. La qualité du contraste avec la fluorescéine met en évidence l’intensité et la répartition des dommages cornéens, fournissant ainsi un aperçu diagnostique précis de la gravité de l’atteinte.
126Les causes d’hyposécrétion lacrymale sont rattachées :
- • le plus souvent à une involution des glandes lacrymales liée à l’âge, à une origine iatrogène médicamenteuse (notamment les anticholinergiques) ou à une altération de l’arc réflexe;
- • parfois à la destruction progressive des glandes lacrymales au cours d’un syndrome de Gougerot-Sjögren, plus rarement d’une réaction du greffon contre l’hôte ou d’une atteinte radique.
Les causes d’altérations lacrymales qualitatives sont liées :
- • à une hyper-évaporation par dysfonctionnement meibomien au cours de la rosacée +++ ou d’autres atteintes inflammatoires meibomiennes chroniques, d’application prolongée de conservateurs ou de prise d’isotrétinoïne;
- • à un déficit de la composante muqueuse lors des atteintes conjonctivales inflammatoires ou fibrosantes (pemphigoïde cicatricielle oculaire, nécrolyse épidermique, brûlure chimique), d’infections locales étendues ou d’agressions environnementales importantes.
![]() La prise en charge de la sécheresse oculaire repose en premier lieu sur :
La prise en charge de la sécheresse oculaire repose en premier lieu sur :
- • l’instillation de substituts lacrymaux (idéalement sans conservateurs) : collyres parfois appelés larmes artificielles (disponibles en flacons ou en unidoses) ou gels (disponibles en tubes ou en unidoses);
- • l’éviction des facteurs irritants ou aggravants : vapeurs chimiques, tabac, poussière, soleil (lunettes teintées), climatisation, ventilation d’air sec ou air chaud pulsé;
- • l’amélioration de la stabilité lacrymale par des soins de paupières adaptés (chauffage puis massage).
Puis, selon les cas, le traitement peut associer :
- • l’occlusion temporaire ou permanente des points lacrymaux;
- • des traitements locaux corticoïdes en cures courtes ou de la ciclosporine topique en traitement prolongé dans certains cas sélectionnés;
- • des traitements généraux (agonistes cholinergiques muscariniques comme le chlorhydrate de pilocarpine, antibiotiques de type doxycycline ou azithromycine);
- • le port éventuel de lunettes à chambre humide ou de verres scléraux si l’atteinte est sévère.
B 127Épisclérite
![]() Il s’agit d’une inflammation localisée à l’épisclère (située sous la conjonctive). On note une rougeur le plus souvent en secteur ou plus rarement diffuse (e-fig. 6.44 à e-fig. 6.46) qui disparaît après instillation d’un collyre vasoconstricteur (chlorhydrate de phényléphrine ou Néosynéphrine®). La douleur oculaire est modérée.
Il s’agit d’une inflammation localisée à l’épisclère (située sous la conjonctive). On note une rougeur le plus souvent en secteur ou plus rarement diffuse (e-fig. 6.44 à e-fig. 6.46) qui disparaît après instillation d’un collyre vasoconstricteur (chlorhydrate de phényléphrine ou Néosynéphrine®). La douleur oculaire est modérée.
L’examen du segment antérieur est normal, mais la lésion prend parfois un aspect de relief nodulaire.
Il est nécessaire de rechercher une maladie de système d’emblée, comme on le fait dans les sclérites si l’interrogatoire est informatif ou en cas de récidive.
C Sclérite
Il s’agit d’une inflammation localisée au niveau de la sclère, générant des douleurs oculaires importantes dites ciliaires, majorées à la mobilisation du globe, irradiant au-dessus et au pourtour de l’orbite, parfois même dans l’oreille ou la mâchoire. Ces douleurs sont volontiers insomniantes, réveillant le patient en fin de nuit. Dans ce cas, on observe une rougeur plane ou nodulaire, localisée en secteur ou diffuse qui ne disparaît pas à l’instillation du collyre vasoconstricteur. L’existence d’une nécrose sclérale ou celle d’une kératite périphérique ulcérante sont des marqueurs de gravité (fig. 6.47, e-fig. 6.48). Une baisse d’acuité visuelle peut survenir en cas de scléro-uvéite, de sclérite postérieure ou encore d’effusion uvéale liée à la sclérite.

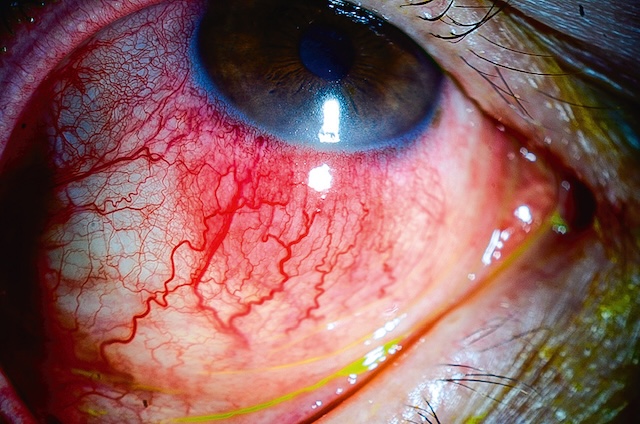
Photographie clinique en lumière blanche concentrée sur le segment antérieur de l’œil droit, révélant une inflammation marquée au niveau de la sclère inférieure. Une congestion intense des vaisseaux épiscléraux forme un réseau vasculaire dilaté et tortueux, avec une zone centrale de surélévation clairement visible, indiquant la présence d’un nodule inflammatoire bien circonscrit. L’intensité de la rougeur, localisée profondément sous la conjonctive, contraste avec la limbe non injectée, suggérant une sclérite nodulaire active. Les cils en périphérie, la brillance de la cornée et la coloration jaune résiduelle du cul-de-sac inférieur accentuent l’environnement inflammatoire. Cette image capte la signature visuelle typique d’un processus inflammatoire scléral profond et douloureux.
La sclérite requiert de rechercher une maladie de système ou un processus infectieux sous-jacents. Dans cette situation, l’enquête biologique est obligatoire, tandis que l’interrogatoire et l’examen clinique recherchent des points d’appel particuliers afin d’orienter la démarche diagnostique :
- • signes articulaires : spondylarthrite ankylosante, polyarthrite rhumatoïde, lupus érythéma-teux disséminé;
- • signes vasculaires : périartérite noueuse, granulomatose avec polyangéite (anciennement maladie de Wegener), cryoglobulinémie, plus rarement maladie de Behçet;
- • signes digestifs : maladies inflammatoires chroniques de l’intestin (MICI);
- • signes cutanés : psoriasis, lupus;
- • 128signes bronchopulmonaires : tuberculose, polychondrite atrophiante, plus rarement sarcoïdose;
- • contexte infectieux : herpès ou zona, borréliose, infection locale à pyocyanique.
D Kératite
C’est une atteinte cornéenne unique ou multiple à type d’altération épithéliale, d’ulcération superficielle ou d’infiltration tissulaire (fig. 6.49) de survenue brutale ou rapide et très symp-tomatique dans sa présentation aiguë, ou plus torpide et aux conséquences optiques souvent majorées au cours des formes chroniques.

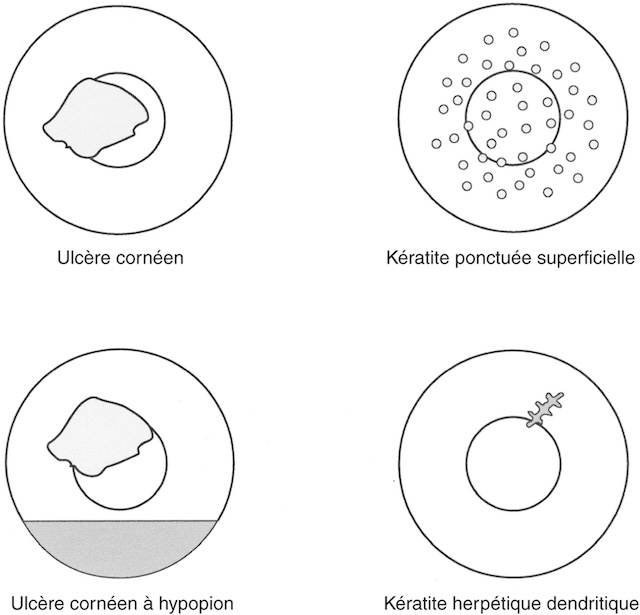
Illustration médicale en noir et blanc présentant de manière schématique quatre types distincts de kératites observées en ophtalmologie. En haut à gauche, l’image montre un ulcère cornéen classique sous forme d’une lésion irrégulière bien délimitée au centre de la cornée. À droite, la kératite ponctuée superficielle est représentée par une multitude de petits points dispersés dans la zone centrale, traduisant des microérosions éparses de l’épithélium. En bas à gauche, l’ulcère cornéen à hypopion associe une même lésion ulcéreuse à un niveau de liquide inflammatoire dense visible dans la chambre antérieure. Enfin, en bas à droite, la kératite herpétique dendritique est illustrée par un motif arborescent finement ramifié situé à la périphérie de la cornée, typique d’une infection herpétique. L’ensemble synthétise visuellement les différences morphologiques entre ces affections cornéennes.
Une kératite aiguë se manifeste par :
- • une baisse d’acuité visuelle d’importance variable suivant la localisation de l’atteinte cor-néenne par rapport à l’axe visuel;
- • des douleurs oculaires pouvant être intenses, à type de sensation de corps étranger, de piqûre, de déchirure ou d’arrachement superficiel;
- • un larmoiement réflexe;
- • une photophobie parfois majeure;
- • un blépharospasme difficile à réprimer.
L’examen à la lampe à fente sera facilité par l’instillation ponctuelle d’une à deux gouttes d’anesthésiques topiques (oxybuprocaïne ou tétracaïne), mais en aucun cas ces derniers ne doivent être prescrits de façon répétitive et prolongée sous peine de complications graves de type perforation cornéenne. Il retrouve des érosions ou des ulcérations de la cornée (fig. 6.50, fig. 6.51, e-fig. 6.52, fig. 6.53 et fig. 6.54 ), une diminution de transparence cornéenne souvent située en regard de l’ulcération et un cercle périkératique (voir plus haut « Examen clinique oculaire »); la chambre antérieure est de profondeur et d’aspect normaux ou peut être le siège d’une réaction inflammatoire dans les cas sévères.
), une diminution de transparence cornéenne souvent située en regard de l’ulcération et un cercle périkératique (voir plus haut « Examen clinique oculaire »); la chambre antérieure est de profondeur et d’aspect normaux ou peut être le siège d’une réaction inflammatoire dans les cas sévères.

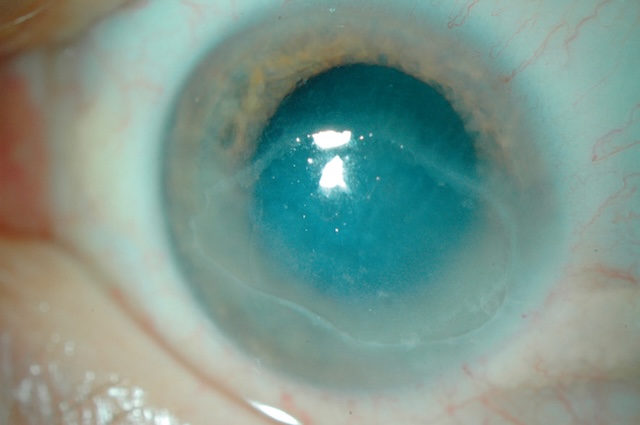
Cette image en lumière directe avec grossissement biomédical met en évidence un ulcère cornéen épithélial, caractérisé par une perte de transparence localisée au centre de la cornée. On y observe une opacification blanchâtre diffuse, irrégulièrement bordée, traduisant une atteinte de la couche épithéliale cornéenne. Le lit ulcéreux est bien délimité, avec un contraste net entre la zone lésée et les tissus cornéens sains environnants. Un discret halo inflammatoire périphérique accompagne la lésion, avec une hyperréflectivité centrale qui capte la lumière incidente. L’ensemble évoque une atteinte infectieuse ou traumatique en phase active, avec une surface cornéenne fragilisée exposée au risque de perforation ou de surinfection. La limbe apparaît globalement respecté, et l’iris, bien que flouté par la turbidité cornéenne, reste discernable. Cette vue rapprochée permet une évaluation précise de la profondeur et de l’étendue de l’ulcération.

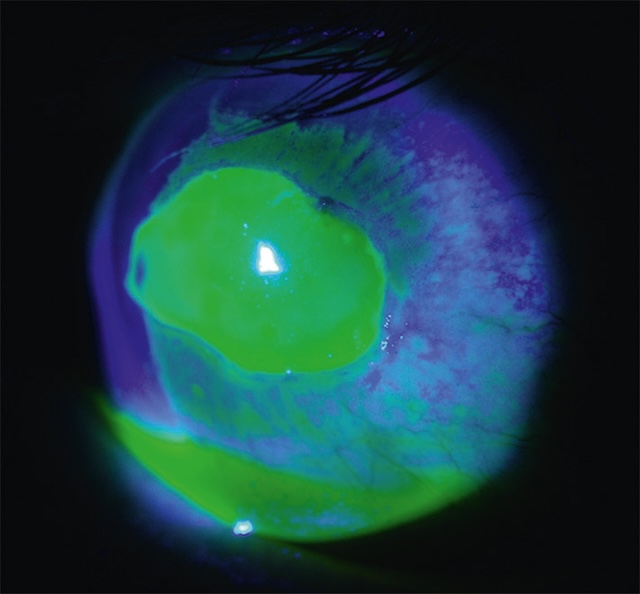
Ce cliché médical réalisé sous lumière bleue après instillation de fluorescéine met en évidence une large atteinte épithéliale cornéenne. L’intense coloration vert fluorescent signale une ulcération étendue de la surface cornéenne, dont les contours sont irréguliers et bien marqués. La fluorescéine, fixée aux zones de dénudation de l’épithélium, révèle ici une perte de continuité importante de la couche protectrice, ce qui oriente fortement vers une kératopathie sévère. L’éclat intense du reflet lumineux au centre accentue la brillance du colorant, tandis que le limbe montre également une hyperfluorescence partielle, suggérant une extension périphérique. L’image provient manifestement d’un examen à la lampe à fente avec filtre cobalt, technique standard en ophtalmologie pour explorer les lésions de la cornée.

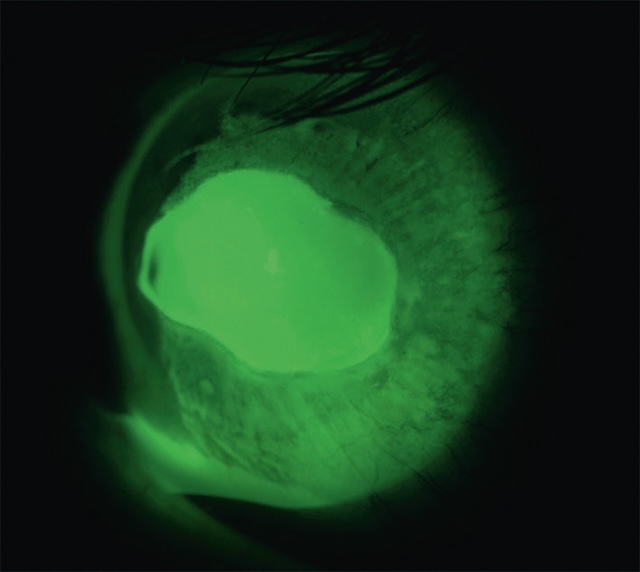
Image capturée en biomicroscopie avec fluorescéine, lumière bleue cobalt et filtre jaune, révélant une large perte épithéliale centrale cornéenne. La zone de défect apparaît comme une lueur verte homogène, parfaitement délimitée au centre de la cornée, traduisant une absence complète d’épithélium à cet endroit. Autour de cette zone centrale, la surface cornéenne présente des microcolorations irrégulières en mosaïque, signe d’un épithélium fragilisé. Les cils sont partiellement visibles en partie supérieure, soulignant l’orientation palpébrale de l’image. L’intensité de la coloration et la netteté des contours suggèrent une lésion franche, probablement traumatique ou infectieuse, nécessitant une surveillance étroite pour prévenir les complications stromales.

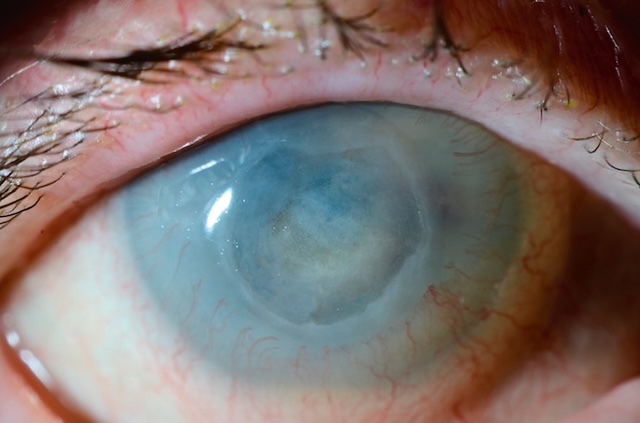
Photographie clinique en haute résolution d’un œil humain, capturant un ulcère cornéen chronique profondément creusant. La cornée présente un aspect opacifié et irrégulier, avec une perte marquée de transparence au centre, traduisant une atteinte stromale avancée. On note une vascularisation anormale à la périphérie cornéenne, visible par la présence de fins vaisseaux rouges s’infiltrant depuis le limbe vers les zones habituellement avasculaires. L’épithélium semble altéré, la surface est granuleuse et inégale, et les tissus environnants sont légèrement congestifs. Ce tableau est typique d’une inflammation prolongée et mal cicatrisée, évoluant vers une néovascularisation secondaire à la chronicité de l’ulcération.
1 129130Kératites infectieuses
Une kératite peut compliquer une conjonctivite à adenovirus (voir plus haut « Conjonctivites virales »); on parle de kératoconjonctivite à adenovirus ou de kératoconjonctivite épidémique. Elle est caractérisée par des petites ulcérations épithéliales disséminées prenant la fluorescéine (fig. 6.55).

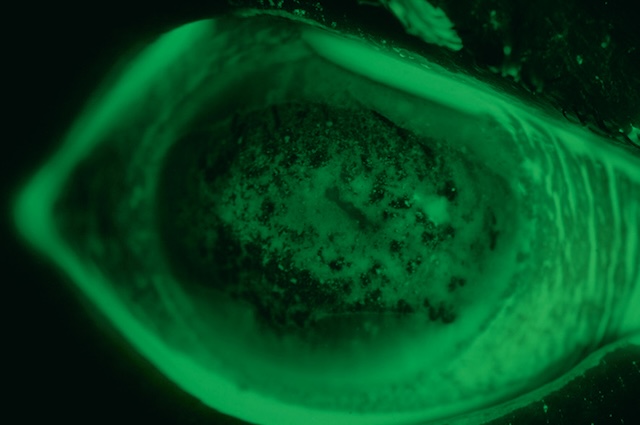
Photographie en lumière bleue après instillation de fluorescéine, montrant avec netteté les premiers signes d’une kératite épithéliale à adénovirus. On distingue, sur l’aire centrale de la cornée, une multitude de micro-atteintes punctiformes, formant un tapis irrégulier d’hyperfluorescence caractéristique. La surface cornéenne semble granuleuse, avec des zones de décollement de l’épithélium marquées par des accumulations fluorescentes. Ces altérations, bien qu’encore superficielles, traduisent déjà une phase inflammatoire active, typique du stade précoce de l’infection virale. La répartition diffuse et non uniforme des lésions sur la cornée centrale, ainsi que la préservation du limbe et de la conjonctive dans cette vue focalisée, renforcent le diagnostic de kératite adénovirale débutante. L’image restitue fidèlement l’aspect clinique en lumière filtrée, précieux pour détecter les lésions précoces souvent peu visibles en lumière naturelle.
131L’évolution est souvent favorable, mais les lésions initiales peuvent laisser place à des opacités stromales antérieures (fig. 6.56) et s’accompagner d’une baisse d’acuité visuelle durable en cas d’opacités cicatricielles centrales.

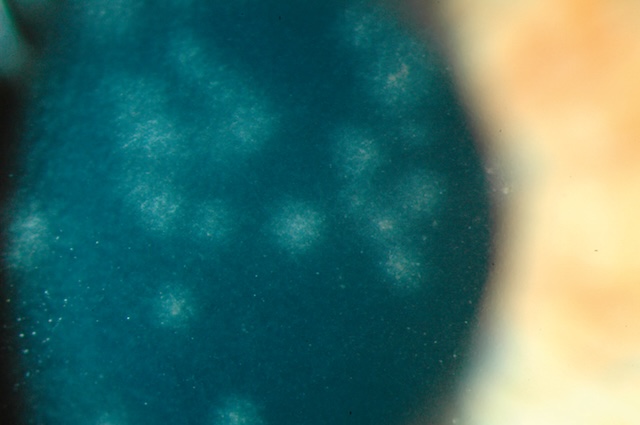
Sur cette photographie réalisée en macrophotographie oculaire avec un grossissement élevé à la lampe à fente, on distingue nettement plusieurs opacités rondes, blanchâtres et bien circonscrites, localisées au sein du stroma cornéen. Ces points diffus, répartis de façon éparse, sont caractéristiques de la phase inflammatoire d’une kératite à adénovirus. Ils témoignent d’un dépôt immunitaire ou d’une infiltration inflammatoire post-virale, souvent responsable d’une baisse de l’acuité visuelle et d’un éblouissement. À droite de l’image, la transition vers une zone plus claire évoque la périphérie cornéenne ou la sclère adjacente, contrastant nettement avec l’aspect trouble central. Le cliché met en valeur une lésion typique dans un contexte post-infectieux, renforçant l’importance du diagnostic ophtalmologique précis.
![]() Le traitement de base est le même que pour la conjonctivite à adénovirus. Une cortico-thérapie locale lentement dégressive est souvent proposée pour aider à dissiper des opacités centrales symptomatiques.
Le traitement de base est le même que pour la conjonctivite à adénovirus. Une cortico-thérapie locale lentement dégressive est souvent proposée pour aider à dissiper des opacités centrales symptomatiques.
b Kératite herpétique
![]() Une kératite herpétique se présente classiquement sous la forme d’une ulcération cor-néenne unilatérale d’aspect typique, de forme arborescente dite « en feuille de fougère » qui ^ correspond à l’ulcère herpétique dendritique (fig. 6.57, fig. 6.58 et e-fig. 6.59), ou est parfois plus étendue et moins spécifique avec des angulations néanmoins évocatrices d’une infection herpétique dites « en carte de géographie » (fig. 6.60 et e-fig. 6.61).
Une kératite herpétique se présente classiquement sous la forme d’une ulcération cor-néenne unilatérale d’aspect typique, de forme arborescente dite « en feuille de fougère » qui ^ correspond à l’ulcère herpétique dendritique (fig. 6.57, fig. 6.58 et e-fig. 6.59), ou est parfois plus étendue et moins spécifique avec des angulations néanmoins évocatrices d’une infection herpétique dites « en carte de géographie » (fig. 6.60 et e-fig. 6.61).

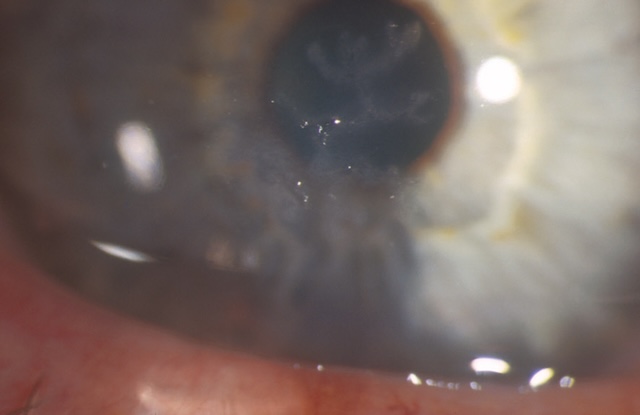
Photographie en biomicroscopie du segment antérieur d’un œil, mettant en évidence une kératite herpétique active. Au centre de la cornée, une lésion arboriforme fine, légèrement en relief, aux contours ramifiés caractéristiques, est visible — typique d’un ulcère dendritique provoqué par le virus herpès simplex. La surface cornéenne semble irrégulière et légèrement œdémateuse autour de la zone infectée, tandis que l’iris reste bien défini avec son motif radial. La transparence partiellement altérée de la cornée laisse deviner une réaction inflammatoire en profondeur. Cette image traduit une atteinte virale localisée mais significative, nécessitant une prise en charge rapide pour prévenir une extension stromale.


Photographie prise à la lampe à fente après instillation de fluorescéine, éclairage par lumière bleue cobalt et filtrage jaune, mettant en évidence un ulcère dendritique typique de la kératite herpétique. Sur la cornée, une lésion ramifiée en forme d’arbre nerveux se dessine clairement, avec un tronc central bien fluorescent d’où émergent de multiples branches sinueuses, caractéristiques du motif dendritique. L’aspect hyperfluorescent correspond à la perte de l’épithélium cornéen le long du trajet viral. Les bords légèrement épaissis accentuent le contraste avec les zones environnantes intactes. L’image reflète une infection active par le virus de l’herpès simplex, dont la présentation morphologique est hautement évocatrice à ce stade.

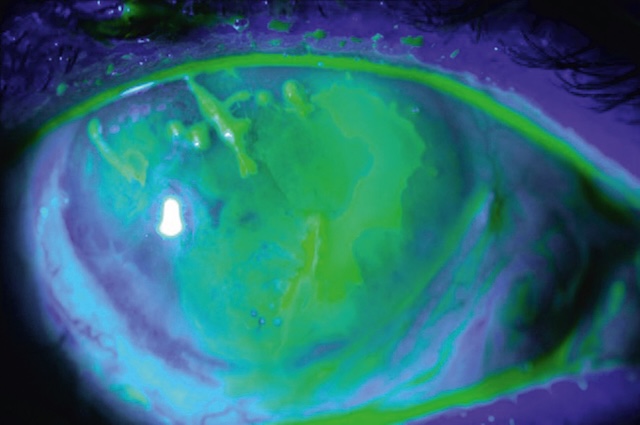
Cette image en lumière bleue après instillation de fluorescéine met en évidence un ulcère géographique herpétique à un stade avancé, avec une surface cornéenne largement altérée. L’ulcération, bien visible par sa coloration vert intense, forme un motif ramifié et étendu aux bords irréguliers, évoquant les contours d’une carte géographique, signe caractéristique de la kératite herpétique. Plusieurs zones apparaissent surélevées ou épaissies, traduisant une nécrose épithéliale active. La cornée montre une perte significative de son intégrité épithéliale, notamment dans les zones centrales et supérieures. Les contrastes fluorescents révèlent des zones de décollement, de fusion lésionnelle, et des extensions en languettes typiques du virus de l’herpès simplex. L’éclairage met en relief les détails topographiques de la surface lésée, soulignant la sévérité de cette atteinte virale. L’aspect global de l’image est hautement évocateur d’un ulcère cornéen herpétique actif.
![]() Un prélèvement pour détection virologique moléculaire peut s’avérer nécessaire dans les formes atypiques ou en cas de résistance thérapeutique avérée.
Un prélèvement pour détection virologique moléculaire peut s’avérer nécessaire dans les formes atypiques ou en cas de résistance thérapeutique avérée.
Le traitement réside dans la prise d’antiviraux par voie générale (valaciclovir ou aciclovir) pendant 7 à 10 jours, associée ou non au débridement initial de la lésion virale. L’alternative consiste, en fonction des situations, en une application locale de même durée d’antiviraux en pommade (aciclovir), en gel (ganciclovir) ou en collyre (trifluridine).
![]() Les kératites herpétiques sont susceptibles de s’aggraver de façon majeure sous l’effet d’une corticothérapie locale inappropriée, pour aboutir dans le pire des cas à une perforation cornéenne. Il faut donc systématiquement écarter le diagnostic de kératite herpétique active (et de façon plus générale celui de kératite infectieuse) avant de débuter une corticothérapie locale sur un œil inflammatoire.
Les kératites herpétiques sont susceptibles de s’aggraver de façon majeure sous l’effet d’une corticothérapie locale inappropriée, pour aboutir dans le pire des cas à une perforation cornéenne. Il faut donc systématiquement écarter le diagnostic de kératite herpétique active (et de façon plus générale celui de kératite infectieuse) avant de débuter une corticothérapie locale sur un œil inflammatoire.
Sous traitement adéquat, la kératite herpétique évolue favorablement dans la majorité des cas. Il existe néanmoins un risque non négligeable d’une part de récidives virales ![]() motivant alors une prophylaxie antiherpétique orale,
motivant alors une prophylaxie antiherpétique orale, ![]() et d’autre part d’évolution vers une kératite plus profonde avec atteinte stromale inflammatoire disciforme (fig. 6.62)
et d’autre part d’évolution vers une kératite plus profonde avec atteinte stromale inflammatoire disciforme (fig. 6.62) ![]() requérant cette fois l’application de corticoïdes locaux sous peine d’opacification cornéenne aux conséquences optiques définitives (voir chapitre 10).
requérant cette fois l’application de corticoïdes locaux sous peine d’opacification cornéenne aux conséquences optiques définitives (voir chapitre 10).

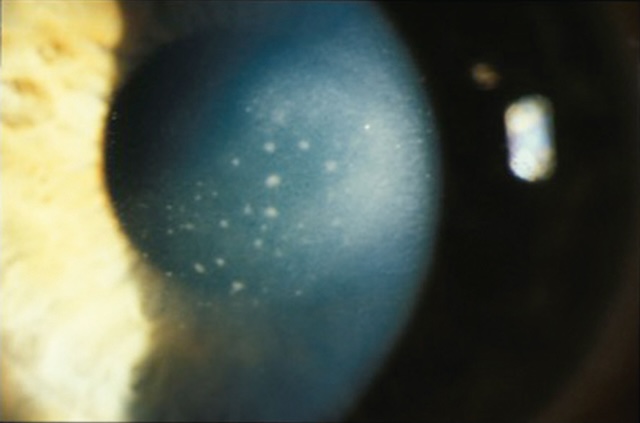
Image en lampe à fente capturant une vue rapprochée de la cornée centrale, révélant une kératite stromale disciforme associée à une kérato-uvéite. La cornée présente un œdème central bien délimité en forme de disque, légèrement bombé, donnant un aspect flou et bleuté à travers le stroma. Plusieurs précipités rétrocornéens fins et blanchâtres sont éparpillés sur l’endothélium, caractéristiques d’une inflammation intraoculaire sous-jacente. L’iris reste partiellement visible en périphérie, mais la zone optique est nettement altérée par l’opacification stromale. Ce cliché illustre une réponse inflammatoire localisée mais intense, souvent observée dans les formes immunitaires de kératite herpétique à expression postérieure.
c 132133Kératite zostérienne
![]() Le zona ophtalmique (fig. 6.63) peut également provoquer des lésions cornéennes :
Le zona ophtalmique (fig. 6.63) peut également provoquer des lésions cornéennes :

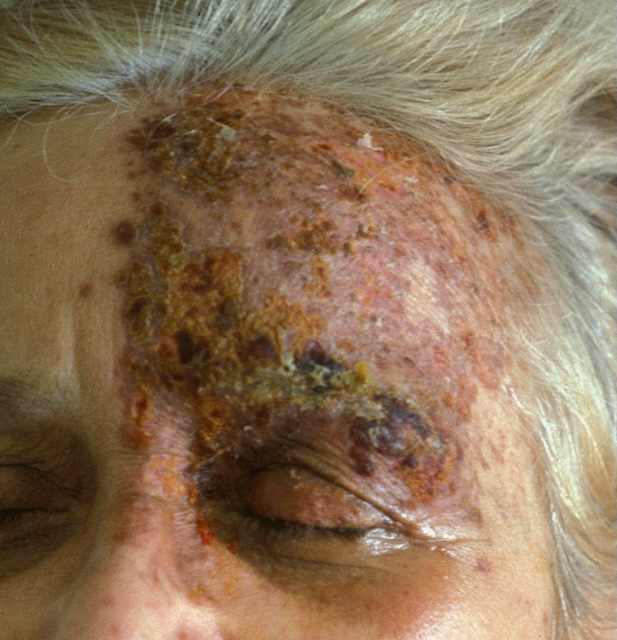
Photographie clinique en lumière naturelle montrant une patiente âgée avec un zona ophtalmique en phase active, localisé sur l’hémiface droite. La peau du front, de la paupière supérieure et de la tempe présente des lésions croûteuses épaisses, brunâtres à noirâtres, mêlées à des zones érythémateuses et suintantes, traduisant une nécrose cutanée évolutive. Le dessin métamérique strictement unilatéral, respectant la ligne médiane du visage, est typique d’une atteinte du dermatome ophtalmique du nerf trijumeau. La paupière est partiellement tuméfiée et collée, suggérant une potentielle atteinte oculaire sous-jacente. Cet aspect témoigne d’une réactivation sévère du virus varicelle-zona, nécessitant une prise en charge rapide pour prévenir les complications oculaires.
- • à type de kératites superficielles dendritiformes (aussi appelées plaques virales), contemporaines de l’épisode aigu du zona, directement liées à l’atteinte virale et répondant à son traitement;
- • à type de kératite neurotrophique (aussi appelée kératite neuroparalytique), plus à distance de l’éruption zostérienne, secondaire à l’anesthésie cornéenne séquellaire
 et de traitement plus délicat.
et de traitement plus délicat.
Instauré précocement dans les trois premiers jours du zona ophtalmique, un traitement par vala-ciclovir (Zelitrex® ou générique) à la posologie de 3 fois 1 g/j permet non seulement le traitement de l’infection virale, mais aussi la réduction de fréquence et de durée des douleurs zostériennes. Un traitement protecteur cornéen local par substituts lacrymaux est systématiquement associé.
![]() Comme dans l’herpès, des complications inflammatoires stromales post-zostériennes sont possibles.
Comme dans l’herpès, des complications inflammatoires stromales post-zostériennes sont possibles.
d Kératites bactériennes, mycosiques et parasitaires
Ces kératites infectieuses surviennent le plus souvent sur un terrain fragilisé par un port inadapté d’une lentille de contact, un traumatisme épithélial cornéen récent (coup d’ongle, branche d’arbre, corps étranger), des troubles de l’anatomie palpébrale (entropion, ectropion, exposition cornéenne paralytique) ou des modifications immunologiques locales d’origine 134iatrogène (corticothérapie prolongée, immunosuppression) qui vont alors réduire l’efficacité des moyens de défense de la surface oculaire.
La situation pratique la plus fréquemment rencontrée est celle d’une infection cornéenne sur défaut évident de port ou d’entretien d’une lentille souple.
Les kératites infectieuses à pyogènes sont caractérisées par la présence d’une plage blanchâtre d’infiltration cornéenne donnant un tableau d’abcès de cornée. Une ulcération est retrouvée à son contact et se colore après instillation de fluorescéine. Elle est parfois aussi accompagnée d’un hypopion réactionnel, témoin d’une inflammation intraoculaire de contiguïté (fig. 6.64, e-fig. 6.65 à e-fig. 6.70).

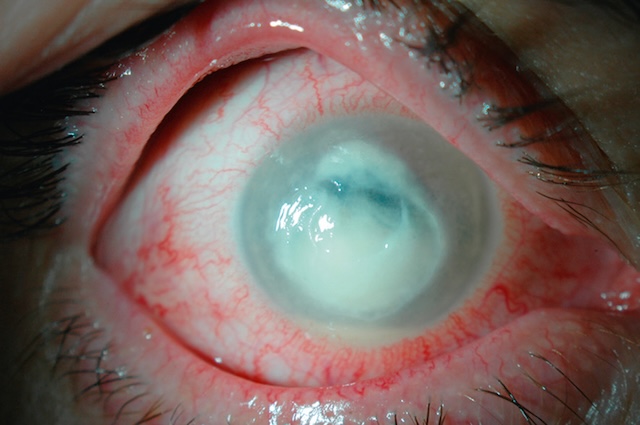
Photographie clinique d’un œil en gros plan montrant un ulcère cornéen infectieux profondément infiltré, associé à un hypopion bien visible. La cornée centrale présente un large infiltrat blanchâtre dense, traduisant une accumulation massive de cellules inflammatoires. En chambre antérieure, une couche horizontale de pus, l’hypopion – est clairement observable, déposée par gravité. Les vaisseaux conjonctivaux sont dilatés, injectant l’œil d’un rouge marqué, signe d’une réponse inflammatoire intense. L’ensemble témoigne d’un tableau sévère et aigu d’infection cornéenne avec franchissement de la barrière endothéliale, nécessitant une prise en charge rapide pour préserver l’intégrité oculaire.
![]() Un prélèvement est effectué au niveau de l’abcès (fig. 6.71 et e-fig. 6.72
Un prélèvement est effectué au niveau de l’abcès (fig. 6.71 et e-fig. 6.72 ) pour examen direct, mise en culture et réalisation d’un antibiogramme ou d’un antifongigramme. Une recherche du pathogène en biologie moléculaire peut compléter les analyses conventionnelles.
) pour examen direct, mise en culture et réalisation d’un antibiogramme ou d’un antifongigramme. Une recherche du pathogène en biologie moléculaire peut compléter les analyses conventionnelles.

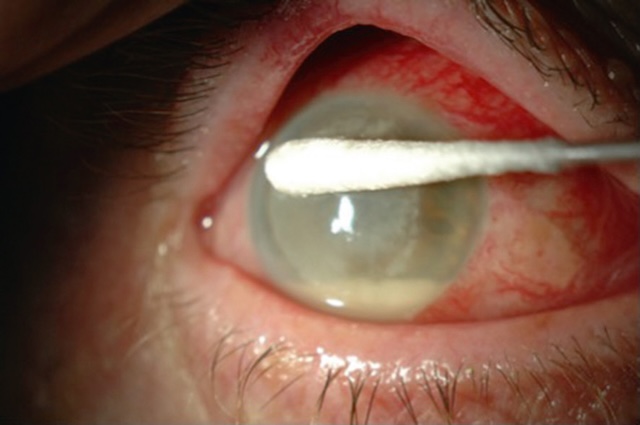
Cette photo médicale en très gros plan documente un prélèvement à l’écouvillon réalisé directement sur la surface cornéenne d’un œil présentant un abcès bien formé. On observe clairement un infiltrat blanc nacré au centre de la cornée, typique d’une accumulation de cellules inflammatoires et d’agents pathogènes, souvent d’origine bactérienne ou fongique. L’écouvillon est appliqué avec précision sur la zone infectée afin de recueillir un échantillon en vue d’une analyse microbiologique. La conjonctive est nettement injectée, signe de l’intensité de la réponse inflammatoire. Ce geste délicat, réalisé sous contrôle visuel, est crucial pour orienter le diagnostic étiologique et adapter le traitement antibiotique ou antifongique.
![]() Parmi les infections bactériennes sous lentilles, le bacille pyocyanique est prépondérant et donne souvent des lésions symptomatiques et destructrices. Les habituels cocci à Gram positif (staphylocoques, streptocoques) sont aussi fréquemment impliqués.
Parmi les infections bactériennes sous lentilles, le bacille pyocyanique est prépondérant et donne souvent des lésions symptomatiques et destructrices. Les habituels cocci à Gram positif (staphylocoques, streptocoques) sont aussi fréquemment impliqués.
Dans tous les cas, le traitement doit être instauré précocement. Il est initialement empirique, puis secondairement adapté aux résultats microbiologiques si nécessaire. Des antibiotiques topiques commercialisés administrés plusieurs fois par jour sont souvent suffisants dans les formes précoces et peu sévères (ciprofloxacine, tobramycine, rifamycine, azithromycine). Pour les abcès importants (en surface, en profondeur ou centraux), il est préférable d’hospitaliser le patient pour instaurer un traitement intensif et régulier (au mieux horaire) avec des collyres aux principes actifs et à concentrations choisis appelés « collyres fortifiés » (vancomycine, gen-tamycine ou amikacine, ceftazidine ou ticarcilline). Une antibiothérapie par voie systémique est associée en cas de risque de diffusion infectieuse.
Les infections fongiques à Fusarium, Candida et Aspergillus sont plus rares, mais volontiers sévères car elles infiltrent la cornée de proche en proche en surface et en profondeur. La conduite thérapeutique est similaire, mais nécessite cette fois un traitement antifongique spécifique intense et prolongé (amphotéricine B, voriconazole).
La kératite amibienne est également l’apanage des porteurs de lentilles. D’installation insidieuse, elle donne d’abord de simples infiltrations épithéliales linéaires (fig. 6.73) régressives sous traitement antiseptique intensif, mais peut aussi se transformer en la redoutable scléro-kératite annulaire (fig. 6.74) de traitement plus complexe. L’évolution des kératites infectieuses peut être défavorable :

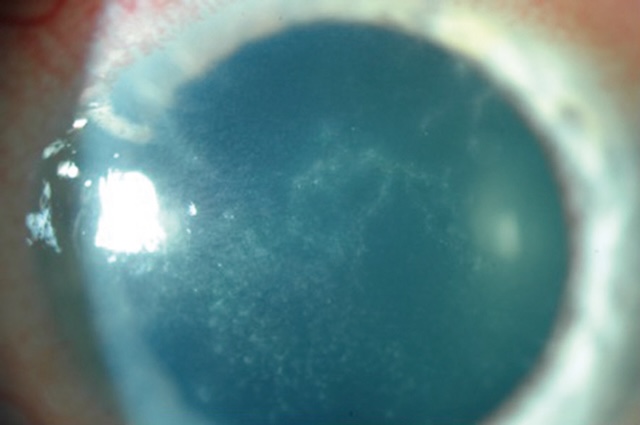
Photographie prise à la lampe à fente montrant un gros plan centré sur la cornée, révélant une kératite amibienne avec atteinte épithéliale linéaire. La surface cornéenne présente un aspect trouble diffus avec des lignes blanchâtres sinueuses à peine visibles, s’étendant de manière radiaire dans le stroma superficiel. Ces traînées linéaires correspondent à des infiltrats typiques du stade précoce d’invasion amibienne. Le reflet lumineux en haut à gauche témoigne d’un œdème cornéen modéré, tandis que la limbe périphérique laisse entrevoir un discret halo inflammatoire. L’image traduit une infection insidieuse, souvent douloureuse, où l’atteinte nerveuse radiaire est un signe d’appel important. Ce tableau est évocateur d’une kératite à Acanthamoeba, fréquente chez les porteurs de lentilles.

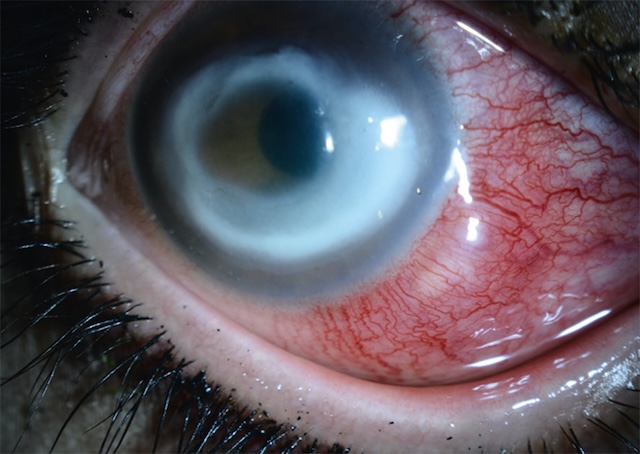
Photographie clinique détaillée d’un œil humain présentant une sclérokératite annulaire d’origine amibienne. On observe une opacification cornéenne marquée, disposée en anneau autour de la zone pupillaire, contrastant avec la transparence centrale résiduelle. Les vaisseaux épiscléraux et conjonctivaux sont intensément dilatés, formant un réseau injecté rouge profond principalement localisé en secteur inférieur. Cette configuration annulaire traduit une inflammation étendue touchant à la fois la cornée et la sclère adjacente, typique d’une atteinte par Acanthamoeba. L'aspect global est évocateur d’un processus infectieux invasif et douloureux, évoluant vers une perte progressive de la clarté cornéenne.
2 Kératites non infectieuses
a Infiltrats inflammatoires non infectieux
De siège préférentiellement périphérique, d’aspect blanchâtre et souvent ulcérés en surface, les infiltrats inflammatoires non infectieux (fig. 6.75) constituent le principal diagnostic 136différentiel des abcès de cornée et sont plus souvent la conséquence de phénomènes inflammatoires locaux (dans un contexte de rosacée oculaire notamment) que le reflet d’une maladie systémique associée.

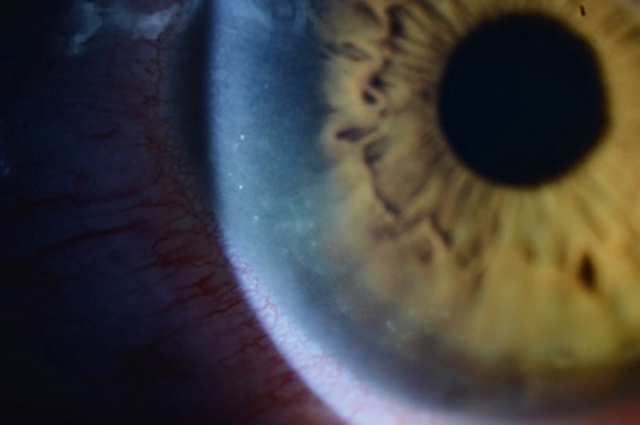
Photographie en lampe à fente avec illumination focalisée, montrant un segment de l’œil en coupe optique, révélant clairement plusieurs infiltrats cornéens périphériques. Ces petites opacités blanchâtres ponctuent le stroma cornéen en zone paracentrale inférieure, suggérant une réponse inflammatoire active. La cornée conserve une certaine transparence en dehors de ces foyers, tandis que la jonction scléro-cornéenne apparaît légèrement congestionnée. L’iris, bien visible avec ses cryptes radiaires, met en contraste les lésions cornéennes par sa netteté. Les infiltrats sont discrets mais multiples, traduisant un processus immunologique ou infectieux modéré, souvent lié à des porteurs de lentilles de contact ou à une hypersensibilité. L’image capte avec précision la localisation périphérique de ces lésions, leur aspect flou et diffus, caractéristiques d’infiltrats précoces ou non ulcératifs.
c Kératite d’exposition
Lors d’une paralysie faciale, la mauvaise occlusion palpébrale est responsable d’une exposition cornéenne induisant une altération épithéliale dans l’aire de la fente palpébrale.
![]() Le traitement réside dans les protecteurs cornéens qui seront d’ailleurs prescrits en prévention dans toutes les situations d’inocclusion.
Le traitement réside dans les protecteurs cornéens qui seront d’ailleurs prescrits en prévention dans toutes les situations d’inocclusion.
Ces kératites peuvent nécessiter une tarsorraphie (affrontement des deux bords libres par mise en place de sutures verticales pour réduire l’étendue de la fente palpébrale), permettant d’assurer la protection de l’épithélium cornéen par la conjonctive palpébrale.
E Uvéite
![]() Le terme d’uvéite se décline de façon anatomique en fonction de la localisation principale ou première du phénomène inflammatoire intraoculaire en cours. Quand le processus touche de manière sensiblement homogène les différents segments du globe oculaire, on parle alors de panuvéite.
Le terme d’uvéite se décline de façon anatomique en fonction de la localisation principale ou première du phénomène inflammatoire intraoculaire en cours. Quand le processus touche de manière sensiblement homogène les différents segments du globe oculaire, on parle alors de panuvéite. ![]() Quels qu’en soient les types anatomiques, les uvéites sont ensuite classiquement séparées en deux grands groupes étiologiques : les uvéites infectieuses et les uvéites non infectieuses, qui diffèrent à la fois dans leurs approches diagnostiques et dans leurs prises en charge thérapeutiques. Enfin, certains diagnostics relèvent d’entités ophtalmologiques définies par un cortège d’éléments cliniques et paracliniques.
Quels qu’en soient les types anatomiques, les uvéites sont ensuite classiquement séparées en deux grands groupes étiologiques : les uvéites infectieuses et les uvéites non infectieuses, qui diffèrent à la fois dans leurs approches diagnostiques et dans leurs prises en charge thérapeutiques. Enfin, certains diagnostics relèvent d’entités ophtalmologiques définies par un cortège d’éléments cliniques et paracliniques.
1 Uvéites antérieures
![]() Les uvéites antérieures sont les formes les plus fréquentes d’uvéites. Elles sont également appelées iridocyclites parce qu’elles touchent la partie antérieure de l’uvée composée de l’iris (iritis) et du corps ciliaire (cyclite).
Les uvéites antérieures sont les formes les plus fréquentes d’uvéites. Elles sont également appelées iridocyclites parce qu’elles touchent la partie antérieure de l’uvée composée de l’iris (iritis) et du corps ciliaire (cyclite).
137Au cours d’une uvéite antérieure aiguë, le patient présente un œil rouge associé à une baisse d’acuité visuelle variable et à des douleurs profondes d’intensité modérée qui irradient vers la région sus-orbitaire.
L’atteinte peut être uni- ou bilatérale, parfois récidivante et à bascule.
L’examen à la lampe à fente retrouve (fig. 6.76) :

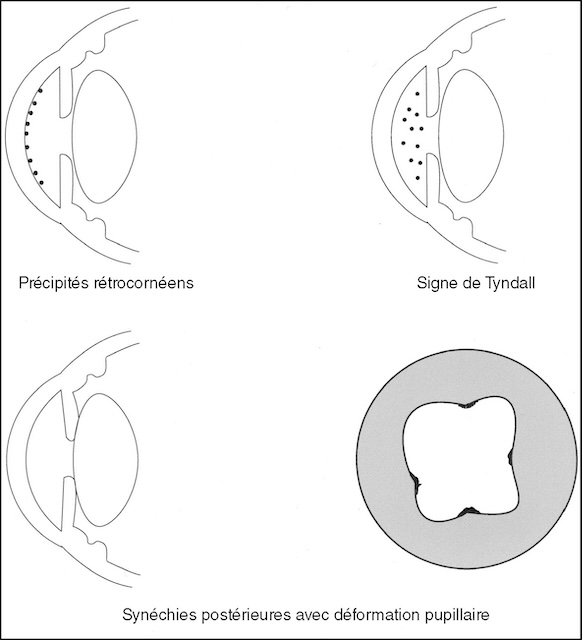
Cette illustration schématique médicale regroupe quatre manifestations classiques d’une uvéite antérieure, mises en évidence de façon précise et pédagogique. En haut à gauche, on observe les précipités rétrocorneens : de petits dépôts cellulaires inflammatoires qui se fixent sur la face postérieure de la cornée, révélateurs d’un processus intraoculaire actif. À droite, le signe de Tyndall est représenté sous forme de particules flottantes dans l’humeur aqueuse, simulant un effet de brouillard lumineux quand il est examiné à la lampe à fente – un marqueur direct de l’inflammation active. En bas à gauche, la présence de synéchies postérieures est illustrée, c’est-à-dire l’adhérence de l’iris au cristallin, souvent responsable d’un blocage pupillaire. Enfin, la dernière image montre clairement une pupille déformée, conséquence de ces synéchies, donnant à l’ouverture pupillaire une forme irrégulière qui traduit un stade avancé de l’uvéite non traitée. Ce type de schéma anatomique est particulièrement utilisé en formation médicale pour illustrer les atteintes caractéristiques des inflammations intraoculaires antérieures.
- • une injection ciliaire périkératique (e-fig. 6.77);
- • une transparence cornéenne normale;
- • une pupille en myosis relatif;
- • parfois des adhérences inflammatoires entre la face postérieure de l’iris et la capsule antérieure du cristallin (« synéchies iridocristalliniennes ou synéchies postérieures) responsables d’une déformation pupillaire qui se dévoile surtout à la dilatation (fig. 6.78);

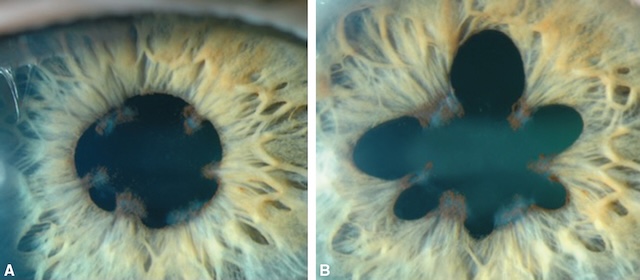
Fig. 6.78 Séquelles d’uvéite antérieure avec synéchies iridocristalliniennes avant (A) et après (B) dilatation. Images cliniques en lumière naturelle montrant une séquelle d’uvéite antérieure avec synéchies iridocristalliniennes avant (image A) et après (image B) dilatation pharmacologique. Sur la première image, la pupille présente une forme irrégulière, légèrement festonnée, avec des zones de contact anormal entre l’iris et le cristallin, indiquant des adhérences postérieures résiduelles. Après dilatation (image B), la pupille ne s’élargit pas de manière homogène, mais révèle une configuration dentelée en marguerite, avec des zones fixées par des synéchies persistantes empêchant l’ouverture complète de l’iris. Ces déformations pupillaires illustrent une fibrose post-inflammatoire, typique des épisodes anciens d’uvéite mal contrôlée. L’architecture irienne reste globalement conservée mais altérée en périphérie par ces attaches cicatricielles.
- • parfois des adhérences inflammatoires entre face antérieure de l’iris et face postérieure de la cornée visibles en gonioscopie (synéchies iridocornéennes ou synéchies antérieures);
- • un phénomène de Tyndall : présence de protéines et de cellules inflammatoires circulant dans l’humeur aqueuse donnant un aspect de phare dans le brouillard à la projection d’un faisceau lumineux de la lampe à fente au travers de la chambre antérieure;
- • des dépôts de cellules inflammatoires sur la face postérieure de la cornée : précipités rétro-cornéens (ou rétrodescemétiques) dont l’aspect morphologique fin (fig. 6.79) ou granulo-mateux (fig. 6.80) permet d’orienter le diagnostic étiologique de l’uvéite.


Fig. 6.79 Uvéite antérieure : précipités rétrocornéens (ou rétrodescémétiques) dits fins. Photographie biomédicale en vue rapprochée de la face postérieure de la cornée, montrant une uvéite antérieure avec présence de précipités rétrocornéens fins, également appelés précipités rétrodescémétiques. L’image restitue une surface trouble, d’aspect flou, uniformément couverte de fines particules disséminées, évoquant une buée interne. Ces dépôts cellulaires s’accumulent sur l’endothélium cornéen en réaction à une inflammation intraoculaire, sans atteinte directe de la structure cornéenne. Leur finesse et leur disposition homogène sont caractéristiques des uvéites d’origine non granulomateuse. Cette apparence voilée illustre parfaitement l’impact visuel perçu par le patient atteint d’une telle inflammation.

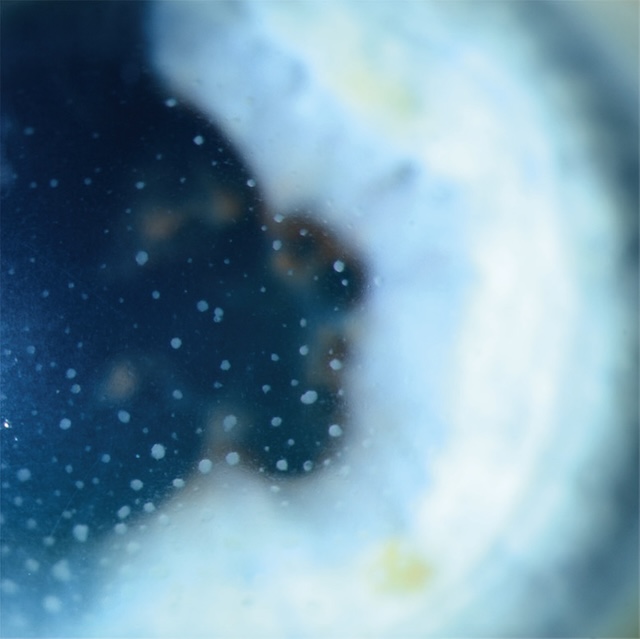
Fig. 6.80 Uvéite antérieure : précipités rétrocornéens dits granulomateux. Photographie en haute définition réalisée à la lampe à fente en lumière focalisée, capturant une uvéite antérieure avec des précipités rétrocornéens dits granulomateux. De multiples dépôts blanchâtres et légèrement bombés sont visibles à la face postérieure de la cornée, formant un voile granuleux diffus. Ces précipités, de tailles variables, s’accumulent surtout en triangle inversé dans la partie inférieure de la cornée, configuration typique en cas d’inflammation intraoculaire d’origine granulomateuse. Le fond pupillaire est obscurci par l’inflammation intraoculaire, et la limpidité habituelle de la chambre antérieure est altérée. L’ambiance visuelle est trouble, traduisant la présence d’un flot cellulaire dans l’humeur aqueuse. Cette image restitue fidèlement l’un des signes classiques de l’uvéite antérieure chronique, souvent associée à des pathologies systémiques comme la sarcoïdose ou la tuberculose.
138139L’examen du segment postérieur comprenant l’étude du vitré et l’analyse du fond d’œil doit être systématique à la recherche d’une atteinte inflammatoire vitréenne (hyalite), rétinienne ou choroïdienne qui signe l’existence d’une uvéite postérieure.
![]() L’enquête étiologique est indispensable, même si elle reste fréquemment négative (un tiers à la moitié des cas). Les principales causes d’uvéites antérieures et leurs archétypes cliniques sont mentionnés ci-après.
L’enquête étiologique est indispensable, même si elle reste fréquemment négative (un tiers à la moitié des cas). Les principales causes d’uvéites antérieures et leurs archétypes cliniques sont mentionnés ci-après.
- • Uvéites non infectieuses associées à des maladies générales :
- – terrain HLA-B27 et spondylarthrite ankylosante ou autre maladie inflammatoire liée au même terrain génétique (MICI, psoriasis, syndrome de Reiter) donnant une uvéite antérieure aiguë unilatérale, d’aspect plastique et synéchiant, souvent à hypopion (fig. 6.81 et e-fig. 6.82), de caractère récidivant et fréquemment à bascule;

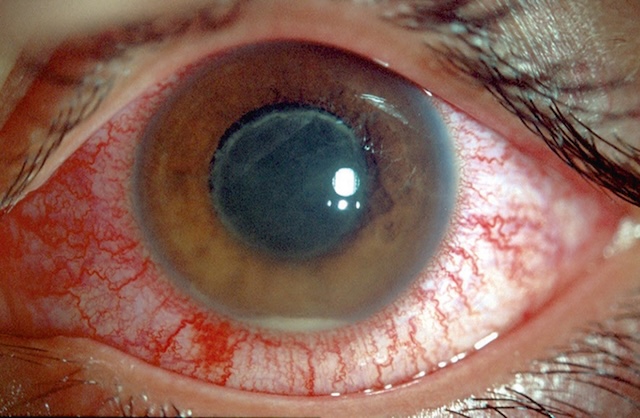
Fig. 6.81 Uvéite antérieure à hypopion avec bouchon cyclitique au cours d’une spondylarthrite ankylosante. Sur cette photographie clinique en haute résolution, on découvre un œil fortement congestionné, où l’hyperhémie conjonctivale est marquée et diffuse, trahissant une inflammation intraoculaire aiguë. Le centre de l’image est dominé par une chambre antérieure trouble, laissant apparaître un hypopion, c’est-à-dire une accumulation de pus stérile au fond de cette chambre, signe franc d’une uvéite antérieure sévère. À cela s’ajoute un bouchon cyclitique visible dans l’axe pupillaire, perturbant la transparence du regard et illustrant une inflammation du corps ciliaire. Le contexte clinique ici évoqué, celui d’une spondylarthrite ankylosante, oriente vers une étiologie auto-immune, classique dans ce type de tableau inflammatoire oculaire. L’iris est légèrement en myosis, piégé par l’activité inflammatoire, et la cornée reste claire mais bordée d’un réseau vasculaire dilaté. Ce type d’image est typique d’un diagnostic d’uvéite antérieure active associée à une maladie systémique.
- – arthrite juvénile idiopathique donnant une uvéite chronique chez l’enfant et de fréquentes complications (cataracte, kératite en bandelette aux dépôts calcifiés blanchâtres ou grisâtres – fig. 6.83 – et glaucome);

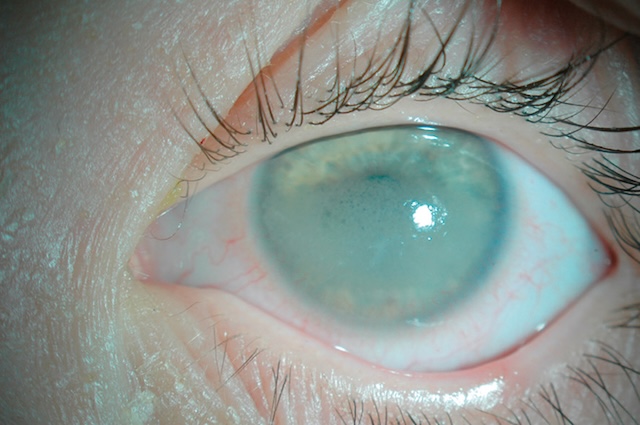
Fig. 6.83 Kératopathie en bandelette sur uvéite antérieure au cours d’une arthrite juvénile idiopathique. Photographie en lumière naturelle d’un œil présentant une kératopathie en bandelette dans le contexte d’une uvéite antérieure chronique associée à une arthrite juvénile idiopathique. La cornée apparaît uniformément trouble avec un voile blanchâtre horizontal, situé dans la partie centrale à supérieure, correspondant à des dépôts de sels calciques dans l’épithélium et le stroma antérieur. La pupille est difficilement visible, masquée par cette opacification cornéenne qui compromet la transparence optique. La sclère et la conjonctive montrent peu de signes d’inflammation active, traduisant une forme ancienne et cicatricielle. Cet aspect est typique des complications oculaires silencieuses mais sévères de l’arthrite juvénile, où l’atteinte cornéenne peut évoluer à bas bruit sans douleur manifeste.
- – sarcoïdose donnant une uvéite dite granulomateuse (dépôts rétrodescemétiques granu-lomateux et nodules iriens fréquents);
- – maladie de Behçet donnant classiquement une uvéite antérieure à hypopion et souvent associée à une atteinte postérieure.
- – terrain HLA-B27 et spondylarthrite ankylosante ou autre maladie inflammatoire liée au même terrain génétique (MICI, psoriasis, syndrome de Reiter) donnant une uvéite antérieure aiguë unilatérale, d’aspect plastique et synéchiant, souvent à hypopion (fig. 6.81 et e-fig. 6.82), de caractère récidivant et fréquemment à bascule;
- • Uvéites infectieuses :
- – uvéite herpétique donnant fréquemment une hypertonie et parfois une atrophie sectorielle de l’iris (fig. 6.84).

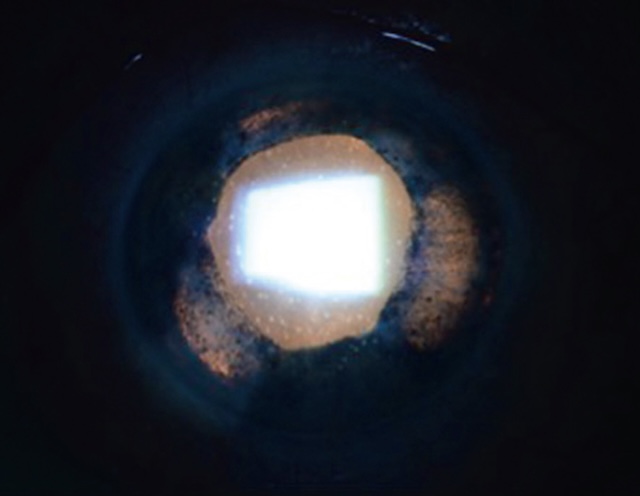
Fig. 6.84 Uvéite herpétique récurrente avec plusieurs zones d’atrophie irienne visibles en rétro-illumination. Image ophtalmologique capturée en rétro-illumination, révélant les stigmates d’une uvéite herpétique récurrente. L’iris laisse transparaître plusieurs zones d’atrophie bien délimitées, visibles sous forme de plages sombres irrégulières contrastant avec la lumière rétroprojetée provenant du fond pupillaire. Ces lacunes tissulaires trahissent une destruction progressive de l’iris, consécutive à des épisodes inflammatoires répétés, typiques des atteintes herpétiques chroniques. La pupille apparaît déformée, irrégulière, et l’ensemble baigne dans un halo lumineux accentuant les contours des lésions atrophiques. Ce type de vue met en évidence les altérations structurelles intraoculaires souvent silencieuses en lumière frontale.
- – uvéite herpétique donnant fréquemment une hypertonie et parfois une atrophie sectorielle de l’iris (fig. 6.84).
La prise en charge de l’uvéite antérieure associe :
2 140Uvéites postérieures
![]() Les uvéites postérieures regroupent les atteintes inflammatoires et infectieuses touchant l’uvée postérieure ou choroïde (choroïdite), la rétine (rétinite) ou les deux tuniques ensemble (choriorétinite ou rétinochoroïdite). La gravité des uvéites postérieures réside initialement dans la possibilité d’une atteinte maculaire, vasculaire ou papillaire irrémédiable aux conséquences fonctionnelles définitives, puis dans la survenue de complications rétiniennes inflammatoires (œdème maculaire cystoïde) ou mécaniques (décollement de rétine tractionnel ou rhegmato-gène) tout aussi redoutables.
Les uvéites postérieures regroupent les atteintes inflammatoires et infectieuses touchant l’uvée postérieure ou choroïde (choroïdite), la rétine (rétinite) ou les deux tuniques ensemble (choriorétinite ou rétinochoroïdite). La gravité des uvéites postérieures réside initialement dans la possibilité d’une atteinte maculaire, vasculaire ou papillaire irrémédiable aux conséquences fonctionnelles définitives, puis dans la survenue de complications rétiniennes inflammatoires (œdème maculaire cystoïde) ou mécaniques (décollement de rétine tractionnel ou rhegmato-gène) tout aussi redoutables.
En fonction des étiologies, l’œil atteint peut avoir un aspect extérieur normal ou présenter une rougeur marquée et des douleurs ciliaires comme au cours des uvéites antérieures. Les symptômes rapportés par le patient sont le plus souvent à type de myodésopsies (décrites comme des points noirs, des mouches volantes ou des corps flottants) ou de baisse d’acuité visuelle (progressive en cas de trouble des milieux ou plus brutale lorsqu’il s’agit d’une atteinte maculaire directe).
L’examen du fond d’œil après dilatation permet de confirmer le diagnostic d’uvéite postérieure, de faire l’inventaire des lésions et de préciser les éventuelles complications. ![]() La démarche étiologique peut alors débuter à partir du constat clinique en s’aidant des éléments retrouvés sur imagerie multimodale et parfois d’arguments biologiques pour arriver au diagnostic final.
La démarche étiologique peut alors débuter à partir du constat clinique en s’aidant des éléments retrouvés sur imagerie multimodale et parfois d’arguments biologiques pour arriver au diagnostic final.
141Les causes d’uvéites postérieures infectieuses sont multiples : toxoplasmose (fig. 6.85), infections à herpès virus (fig. 6.86), dont la rétinite à cytomégalovirus chez l’immunodéprimé, syphilis (fig. 6.87), bartonellose ou encore tuberculose.

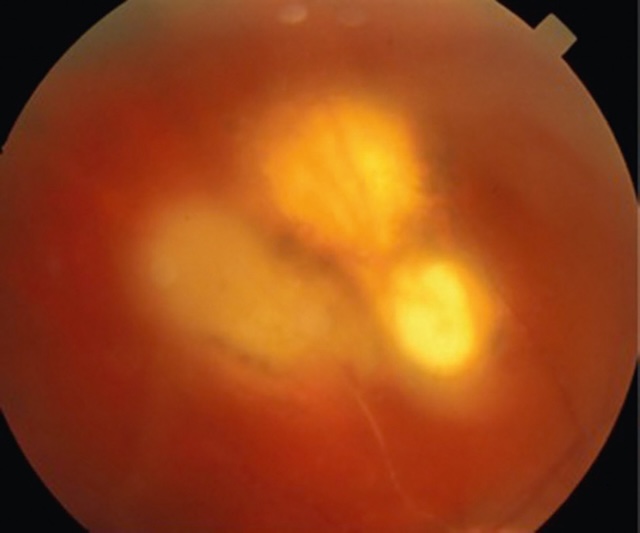
Photographie couleur du fond d’œil prise en rétinographie, illustrant une troisième récidive de toxoplasmose oculaire avec complication vasculaire manifeste. On y distingue une large zone nécrotique rétinienne blanchâtre, d’aspect cotonneux, centrée sur des foyers cicatriciels anciens qui ont pris une teinte jaunâtre. Ces lésions inflammatoires coalescentes contrastent fortement avec l’orange homogène du fond rétinien normal. En haut à droite, une lueur brillante accentue l’activité inflammatoire en cours, tandis qu’un territoire rétinien adjacent paraît ischémié, trahissant une occlusion d’une branche artérielle. Les bords de cette zone ischémique sont flous, traduisant une propagation de l’œdème autour du foyer vasculaire obstrué. L’ensemble de l’image témoigne d’un épisode récurrent sévère, où l’inflammation liée à la toxoplasmose a été aggravée par un phénomène thrombotique local, avec un risque réel d’atteinte visuelle durable.

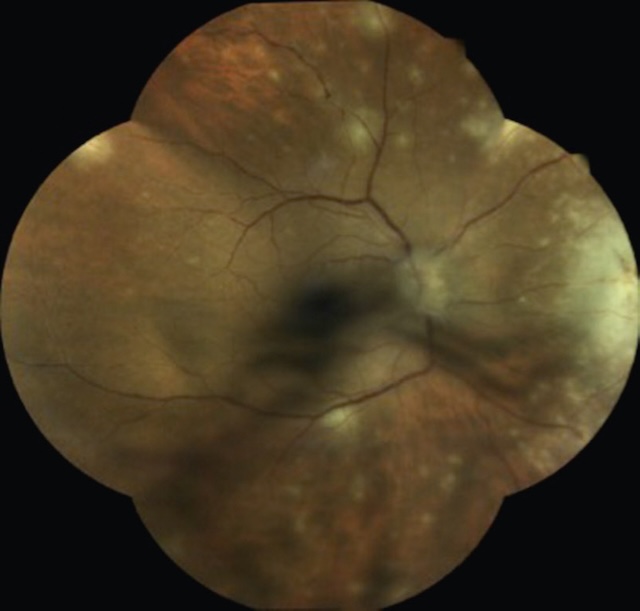
Sur cette photographie rétinienne en grand champ, l’œil droit révèle une atteinte sévère de la rétine, avec de vastes zones blanchâtres en nappe, mal limitées, qui trahissent une nécrose active étendue. Les vaisseaux rétiniens sont déformés, parfois effacés, et traversent des plages atrophiques typiques d’un processus inflammatoire aigu. La région maculaire semble envahie par un halo flou, sans fovéa centrale nette, suggérant une atteinte potentiellement irréversible de la vision centrale. Ce tableau est tout à fait typique d’une nécrose rétinienne aiguë d’origine herpétique, souvent rapide et destructrice si elle n’est pas prise en charge à temps. Ce type d’image, capturé lors d’un fond d’œil, s’inscrit dans un contexte clinique d’urgence, souvent chez un patient immunodéprimé, avec menace directe pour la fonction visuelle. L’aspect hétérogène et la disposition centrifuge des lésions renforcent le diagnostic. Ce n’est pas un simple cliché, c’est une alerte visuelle sur la gravité d’une pathologie silencieuse mais redoutable.

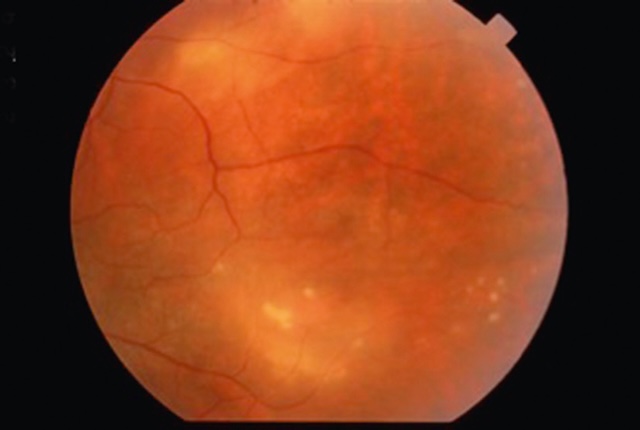
Image de fond d’œil obtenue par rétinographie couleur, centrée sur la périphérie rétinienne, révélant plusieurs foyers blanchâtres et flous disséminés, typiques d’une rétinite syphilitique périphérique. La rétine présente une vascularisation normale en périphérie, mais l’arrière-plan est altéré par des zones d’infiltrat inflammatoire diffus. Certains vaisseaux apparaissent partiellement masqués par les lésions actives, suggérant une atteinte inflammatoire intrarétinienne. L’aspect global est celui d’une inflammation progressive, non exsudative, avec quelques points de cicatrisation discrète. Cette image évoque une atteinte infectieuse systémique à tropisme oculaire, qui impose un diagnostic étiologique rapide et une prise en charge ciblée.
Parmi les causes systémiques d’uvéites postérieures non infectieuses, nous mentionnerons la fréquence de la sarcoïdose (fig. 6.88) et le risque fonctionnel de la maladie de Behçet.

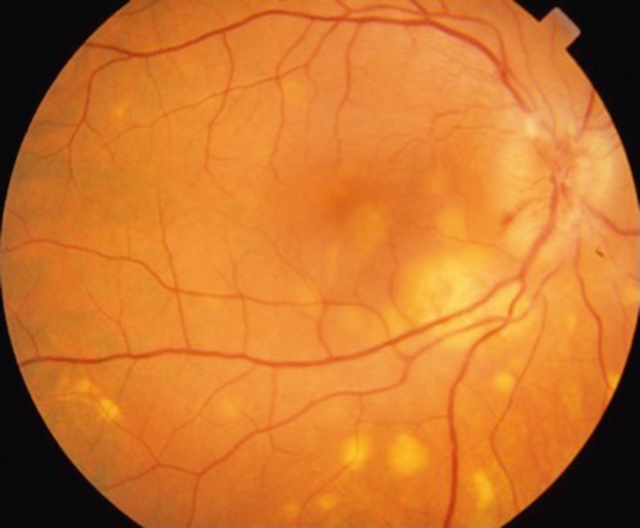
Image de fond d’œil en rétinophotographie couleur illustrant une choroïdite granulomateuse associée à une papillite dans un contexte de sarcoïdose oculaire. On observe plusieurs foyers arrondis, jaunâtres et légèrement surélevés disséminés dans la rétine moyenne et périphérique, correspondant à des granulomes choroïdiens actifs. Le nerf optique, situé en haut à droite, présente des bords flous, trahissant une inflammation du disque optique, typique d’une papillite. Les vaisseaux rétiniens demeurent visibles mais légèrement tortueux, en particulier dans les zones adjacentes aux foyers granulomateux. La macula paraît légèrement estompée, possiblement impactée par l’œdème inflammatoire. Cet aspect multifocal et diffus est très évocateur d’une atteinte sarcoïdosique intraoculaire chronique.
F 142Infection (endophtalmie) postopératoire
![]() Le contexte postopératoire permet d’évoquer une complication d’origine infectieuse. Elle survient le plus souvent quelques jours après une chirurgie de la cataracte, plus rarement après une chirurgie de la rétine ou plus à distance d’une chirurgie du glaucome (fig. 6.89), mais parfois aussi au décours d’une simple injection intravitréenne thérapeutique. Le patient ressent une douleur oculaire intense du côté opéré, qui irradie vers la région sus-orbitaire et s’accompagne d’une baisse visuelle habituellement conséquente. À l’examen, on peut noter l’existence d’un œdème palpébral, celle d’un hypopion ou d’une membrane cyclitique visibles avec la lampe à fente, celle enfin d’une hyalite signant l’inflammation du segment postérieur et qui, selon son importance, limite ou empêche la visualisation du fond d’œil. La réalisation d’une échographie oculaire est alors nécessaire pour obtenir des informations sur l’état du segment postérieur. Une atteinte de la totalité des tuniques oculaires signe la gravissime panophtalmie.
Le contexte postopératoire permet d’évoquer une complication d’origine infectieuse. Elle survient le plus souvent quelques jours après une chirurgie de la cataracte, plus rarement après une chirurgie de la rétine ou plus à distance d’une chirurgie du glaucome (fig. 6.89), mais parfois aussi au décours d’une simple injection intravitréenne thérapeutique. Le patient ressent une douleur oculaire intense du côté opéré, qui irradie vers la région sus-orbitaire et s’accompagne d’une baisse visuelle habituellement conséquente. À l’examen, on peut noter l’existence d’un œdème palpébral, celle d’un hypopion ou d’une membrane cyclitique visibles avec la lampe à fente, celle enfin d’une hyalite signant l’inflammation du segment postérieur et qui, selon son importance, limite ou empêche la visualisation du fond d’œil. La réalisation d’une échographie oculaire est alors nécessaire pour obtenir des informations sur l’état du segment postérieur. Une atteinte de la totalité des tuniques oculaires signe la gravissime panophtalmie.

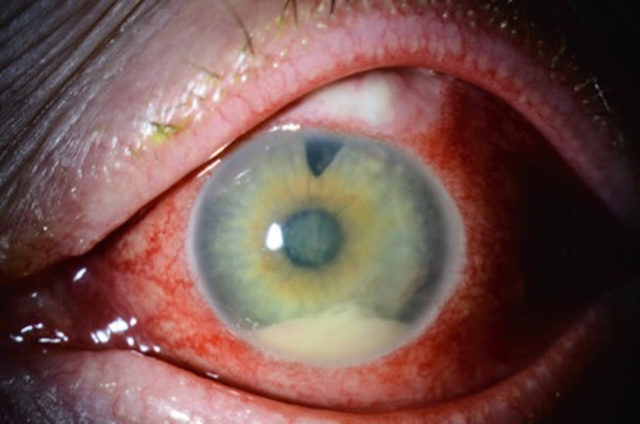
Photographie clinique à fort grossissement d’un œil présentant une endophtalmie tardive sur bulle de filtration conjonctivale après trabéculectomie pour glaucome. L’œil est fortement inflammatoire, avec une injection conjonctivale marquée, un hypopion dense occupant la chambre antérieure, et une opacification cornéenne débutante. La bulle de filtration supérieure est blanchâtre, tendue, et semble surinfectée, marquant un point d’entrée potentiel pour les agents pathogènes. Le regard est figé, avec un iris à peine visible à travers une cornée trouble, traduisant un processus infectieux intraoculaire avancé. L’aspect global évoque une urgence ophtalmologique majeure sur antécédent chirurgical.
![]() Le traitement étiologique impose la réalisation urgente d’injections intravitréennes d’antibiotiques, associée ou non à une antibiothérapie systémique. Un prélèvement de liquide intraoculaire est effectué dans l’instant précédant l’injection intraoculaire des antibiotiques. Il est adressé rapidement au microbiologiste pour examen direct et culture, et complété d’analyses moléculaires quand les techniques sont disponibles. Une vitrectomie est discutée d’emblée dans les cas sévères, ou peut être proposée secondairement pour rétablir une transparence des milieux.
Le traitement étiologique impose la réalisation urgente d’injections intravitréennes d’antibiotiques, associée ou non à une antibiothérapie systémique. Un prélèvement de liquide intraoculaire est effectué dans l’instant précédant l’injection intraoculaire des antibiotiques. Il est adressé rapidement au microbiologiste pour examen direct et culture, et complété d’analyses moléculaires quand les techniques sont disponibles. Une vitrectomie est discutée d’emblée dans les cas sévères, ou peut être proposée secondairement pour rétablir une transparence des milieux.
 Compléments en ligne
Compléments en ligne
Quel diagnostic proposez-vous en première intention devant la survenue brutale d’une rougeur oculaire unilatérale localisée et isolée à type de flaque hématique ?
Parmi les éléments cliniques suivant, quels sont ceux faisant évoquer le diagnostic de kératite ?
Devant un tableau d’œil rouge unilatéral, quel symptôme clinique vous orientera particulièrement vers le diagnostic de sclérite ?
Quel diagnostic évoquez-vous en première intention chez un patient de 70 ans présentant un œil droit rouge et douloureux avec baisse d’acuité visuelle 4 jours après une chirurgie de cataracte homolatérale ?
Vous examinez une lésion cornéenne à la lampe à fente en lumière bleue après instillation de fluorescéine aqueuse. Quels sont les deux types d’ulcération épithéliale permettant de proposer une origine herpétique ?
Le port de lentilles de contact souples favorise la survenue de certaines infections cornéennes, lesquelles ?
 Compléments en ligne
Compléments en ligne
Des compléments numériques sont associés à ce chapitre. Ils sont indiqués dans le texte par un picto. Pour voir ces compléments, connectez-vous sur http://www.em-consulte.com/ e-complements/478662 et suivez les instructions.

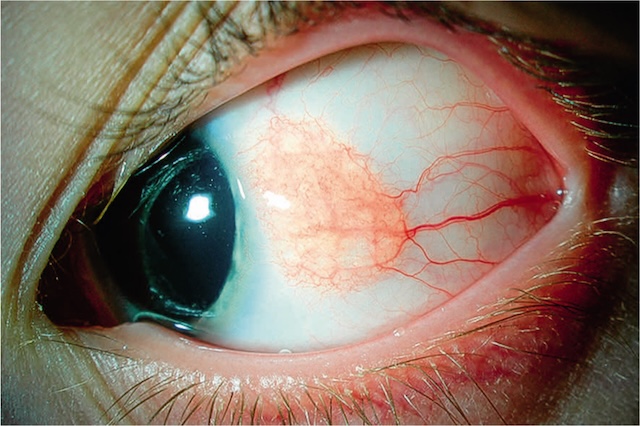
Ce gros plan révèle une rougeur oculaire bien localisée au niveau de la conjonctive bulbaire nasale, attirant immédiatement l’attention par sa teinte rosée diffuse et la densité inhabituelle des vaisseaux engorgés dans la zone. En s’y attardant, on distingue que cette congestion ne correspond pas à une inflammation aiguë ou diffuse classique, mais plutôt à une structure sous-jacente plus épaisse, légèrement surélevée, sans pigmentation foncée visible. C’est typique d’un nævus achrome, une lésion conjonctivale bénigne, souvent présente dès l’enfance et évoluant lentement. Contrairement à son homologue pigmenté, ce type de nævus se manifeste de manière plus discrète, sans coloration brune, mais peut néanmoins provoquer une réaction vasculaire autour, comme c’est visiblement le cas ici. L’œil lui-même est bien blanc en dehors de cette zone, sans signes de kératite ni de réaction en chambre antérieure, ce qui exclut d’emblée une pathologie infectieuse ou inflammatoire plus grave.

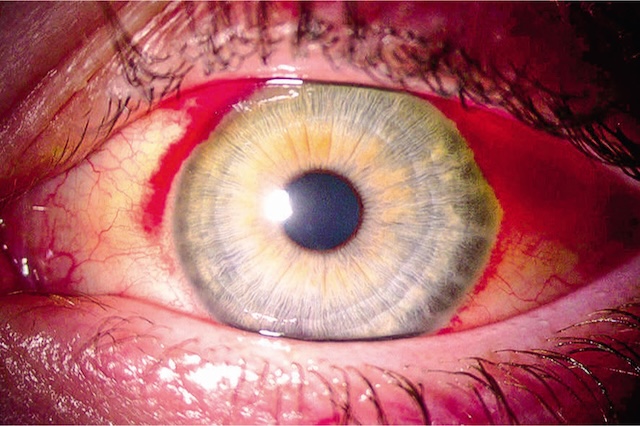
Ce cliché montre un œil parfaitement ouvert, capturé en lumière directe, révélant une zone bien délimitée de rouge vif au niveau de la sclère supérieure, juste sous la conjonctive. Cette nappe rouge en croissant, intense et localisée, ne s’étend pas vers la cornée ni la pupille, ce qui permet de rassurer d’emblée sur son caractère non urgent. Il s’agit ici d’une hémorragie sous-conjonctivale, un petit saignement sous la surface de l’œil, souvent impressionnant à l’œil nu mais bénin dans la majorité des cas. Aucun signe d’inflammation active, pas de larmoiement ni de douleur visible, ce qui est typique de cette situation. L’iris est clair, bien coloré et la pupille centrale, sans déformation ni réaction anormale.
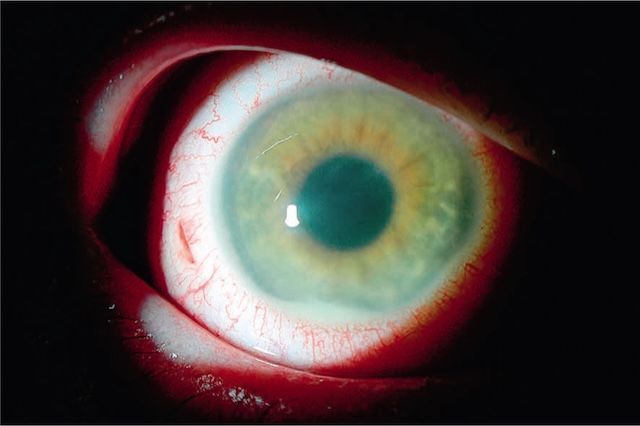
Cette photographie en très gros plan d’un œil révèle une situation préoccupante. L’iris présente des couleurs nuancées, mais ce qui interpelle, c’est cette opacité centrale qui brouille la chambre postérieure, traduisant une atteinte profonde du globe. Les vaisseaux conjonctivaux sont dilatés et injectés, dessinant une rougeur périkératique intense, typique d’une réaction inflammatoire sévère intraoculaire. Cette configuration visuelle évoque fortement la présence d’un corps étranger ayant pénétré jusqu’au segment postérieur, probablement au travers du globe, et ayant déclenché une endophtalmie — une infection intraoculaire grave. L’aspect trouble du segment antérieur laisse présager une diffusion de l’inflammation, voire un envahissement purulent. Ce genre de tableau clinique impose une prise en charge en urgence absolue, car chaque heure compte pour éviter une perte irréversible de la vision.

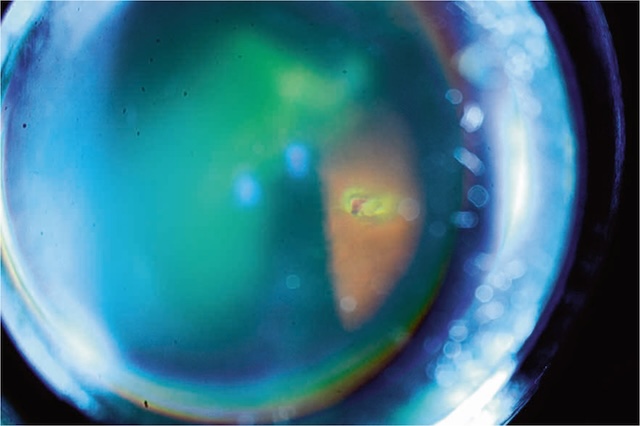
L’image capturée ici montre un œil examiné de très près, vraisemblablement par une lentille spécialisée utilisée en ophtalmologie pour l’examen du segment postérieur. L’attention se porte immédiatement sur une structure réfléchissante visible dans la zone centrale du champ, clairement logée dans le plan rétinien profond. Il s’agit d’un corps étranger intraoculaire postérieur, possiblement métallique, identifiable par son éclat net au sein d’un environnement rétinien altéré. L’arrière-plan révèle une zone d’ombre diffuse autour de l’objet, témoignant d’un effet traumatique localisé. Ce cliché donne aussi une idée de la profondeur et des structures internes de l’œil, avec les contours circulaires de la lentille optique visible autour du champ. L’ensemble suggère un traumatisme pénétrant ancien ou récent avec fixation du fragment dans la rétine, nécessitant une évaluation chirurgicale minutieuse. Le caractère flou en périphérie renforce l’impression d’un grossissement important, comme dans une observation en biomicroscopie avec lentille.

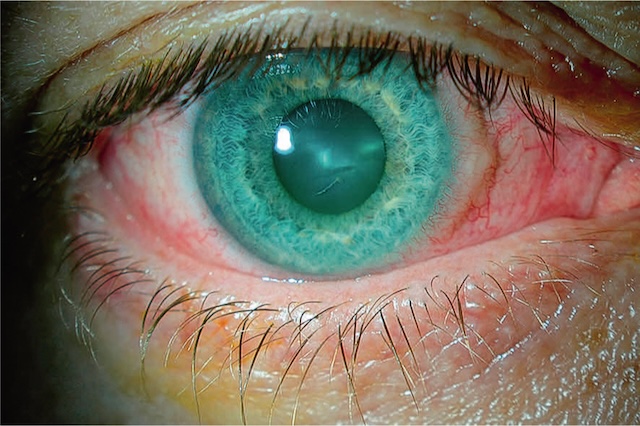
Sur cette photographie en très gros plan, l’œil présente une rougeur conjonctivale marquée, plus accentuée vers la région nasale, signe classique d’irritation ou de traumatisme. La cornée, bien que globalement intacte, montre une plaie étanche, à peine perceptible à l’œil nu, mais suggérée par la texture légèrement altérée de sa surface. En arrière de la pupille, le cristallin trahit une opacification dense et centrale, caractéristique d’une cataracte traumatique. Ce voile blanchâtre dans l’axe visuel contraste fortement avec la transparence habituelle du segment antérieur. L’œil semble douloureux et hyperémique, et le regard fixe indique un inconfort évident. L’ensemble des signes évoque un traumatisme oculaire direct avec atteinte du cristallin, nécessitant une prise en charge ophtalmologique rapide.

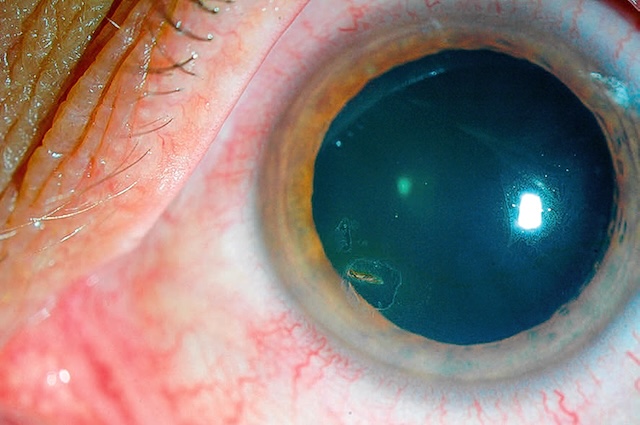
Ce cliché hyper détaillé d’un œil en gros plan attire immédiatement l’attention sur une cornée anormalement brillante mais marquée en son centre par une anomalie bien localisée. On distingue clairement un petit corps étranger métallique logé dans le stroma cornéen, accompagné d’un halo inflammatoire discret autour de la zone d’impact. La structure du métal se dessine comme un minuscule éclat incrusté, laissant deviner un traumatisme oculaire récent, souvent dû à une projection à haute vitesse sans protection. L’aspect limpide du reste de la cornée contraste avec cette zone opaque, soulignant la nature localisée de la lésion. Les vaisseaux conjonctivaux sont légèrement dilatés, témoins d’une réaction inflammatoire modérée. L’image évoque une situation d’urgence ophtalmologique, typique d’un accident de bricolage ou industriel.

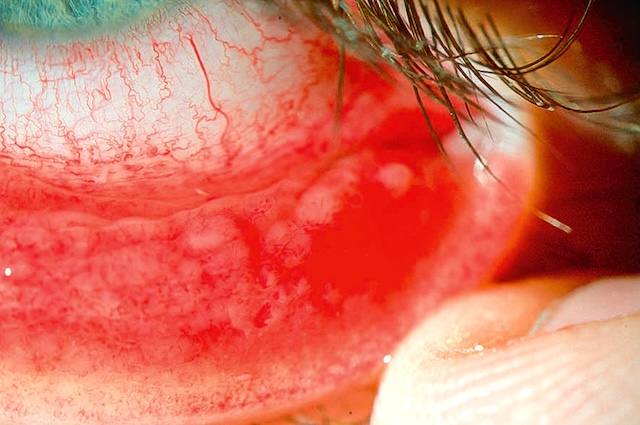
On voit ici l’intérieur de la paupière inférieure, clairement inflammé, avec une rougeur marquée de la conjonctive. Ce qui saute tout de suite aux yeux, ce sont ces petits reliefs blanchâtres bien visibles, regroupés en amas, qui traduisent la présence de follicules. La surface paraît granuleuse, et la vascularisation est nettement accentuée, traduisant une irritation active. Cette image évoque sans détour une conjonctivite folliculaire d’origine infectieuse, comme on en voit souvent avec certaines infections virales ou bactériennes. Ce type d’aspect est typique, facilement reconnaissable quand on sait quoi chercher. La paupière semble légèrement retournée par le doigt du patient ou de l’examinateur, ce qui permet une belle mise en évidence des lésions sans filtre, directement à l’œil nu, dans une lumière franche. C’est une situation fréquente en consultation, qui demande une prise en charge rapide mais bien ciblée.

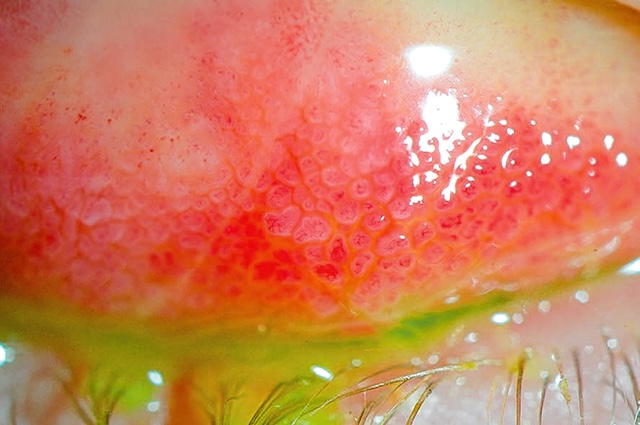
Ce gros plan très net d’une paupière supérieure éversée met en évidence une conjonctivite allergique papillaire, caractérisée par une surface conjonctivale épaissie et parsemée de multiples papilles saillantes et régulières. Ces structures en relief, de forme polygonale bien distincte, confèrent à la conjonctive un aspect pavimenteux typique, souvent comparé à une mosaïque. Le tissu est intensément rouge, témoignant d’une hypervascularisation locale, avec une légère brillance liée à l’écoulement du film lacrymal. Une sécrétion mucoïde verdâtre est visible à la base des cils inférieurs, un signe fréquent dans ce type d’allergie chronique. Cette présentation clinique est très évocatrice d’une allergie oculaire modérée à sévère, fréquemment retrouvée chez les patients atopiques, en particulier au printemps. L’examen a probablement été réalisé à la lampe à fente avec éversion de la paupière pour visualiser la zone tarsale souvent négligée.

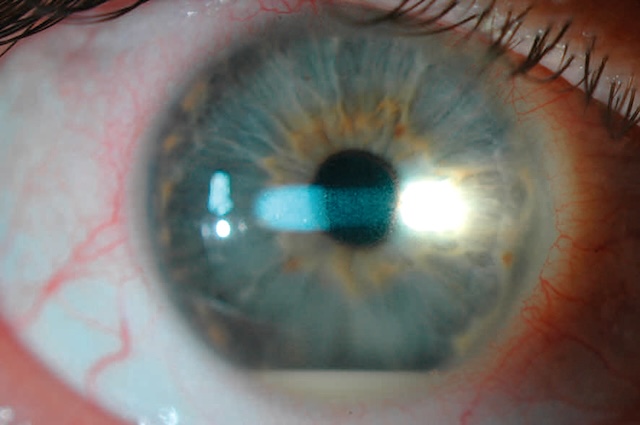
Ce cliché biomédical met en lumière un phénomène clinique bien connu dans les états inflammatoires de l’œil : l’effet Tyndall, ici associé à un hypopion. L’image, capturée à la lampe à fente, révèle un faisceau lumineux qui traverse la chambre antérieure et y déploie une dispersion caractéristique due aux cellules inflammatoires en suspension dans l’humeur aqueuse. Ce halo opalescent est typique d’une uvéite antérieure aiguë. En contrebas, on distingue une accumulation blanche en croissant au niveau inférieur de la chambre antérieure : l’hypopion, témoin d’une réponse inflammatoire intense, traduisant la présence de pus stérile formé par les leucocytes. L’iris, aux teintes bleutées et dorées, reste visible mais légèrement flouté par cette turbidité. L’œil dans son ensemble est injecté de vaisseaux, signalant l’état congestif du segment antérieur. L’image interpelle par son réalisme, capturant une pathologie ophtalmique aiguë avec une précision clinique remarquable.

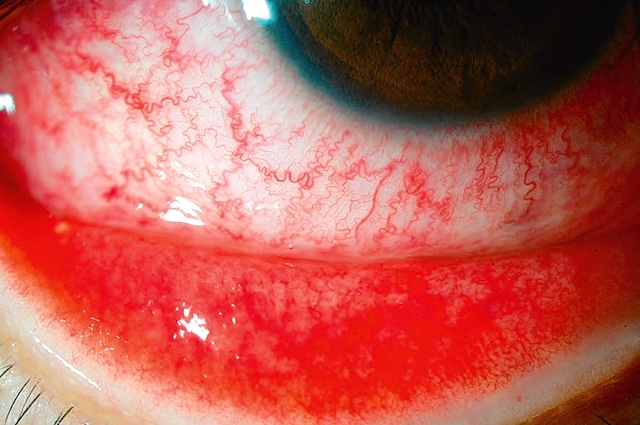
Cette photographie médicale très rapprochée met en évidence une hyperémie marquée de la conjonctive bulbaire et tarsale inférieure, typique d’une conjonctivite virale. On observe une injection conjonctivale diffuse, avec une prédominance de vaisseaux tortueux et dilatés bien visibles, donnant un aspect congestif à l’œil. Le rouge intense, étendu jusqu'à la zone palpébrale inférieure, trahit une inflammation aiguë d’origine virale, souvent accompagnée dans la réalité clinique de larmoiement, photophobie ou sensation de brûlure. L’absence de sécrétions épaisses dans cette vue appuie l’origine virale plutôt qu’allergique ou bactérienne.

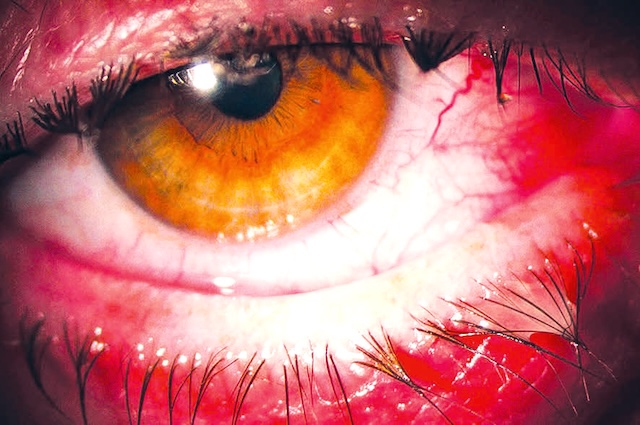
Ce gros plan d’un œil humain, capturé en contexte clinique, illustre les signes caractéristiques d’une conjonctivite. Le regard, à demi-ouvert, révèle une hyperhémie conjonctivale marquée, visible par les vaisseaux sanguins dilatés et tortueux qui serpentent la sclère, témoignant d’une réaction inflammatoire active. Le pourtour des paupières, notamment la partie inférieure, présente une rougeur vive, un léger œdème et une certaine brillance, signes typiques d’irritation conjonctivale aiguë. L’intérieur de la paupière inférieure laisse entrevoir une conjonctive palpébrale épaissie, luisante, marquant une congestion évidente. La coloration jaune ambrée de l’iris contraste vivement avec l’aspect rougeâtre des tissus périphériques, accentuant l’intensité visuelle de l’inflammation. Ce type d’image est clairement une photographie médicale ophtalmologique, focalisée sur la conjonctive.

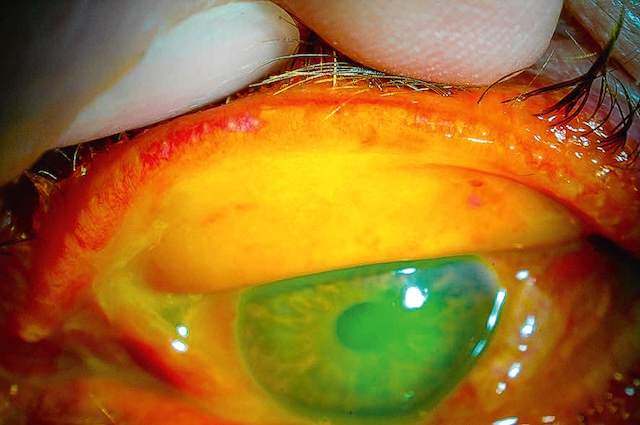
Cette photographie prise à la lampe à fente montre en gros plan l’intérieur de la paupière inférieure, présentant une conjonctive nettement rouge, congestionnée et enflammée. Au centre de l’image, on observe une fausse membrane blanchâtre, fine et légèrement translucide, typiquement plaquée à la conjonctive. Elle est saisie délicatement par une pince, dans un geste d’extraction très précis. Ce genre de membrane est souvent associé à une conjonctivite adénovirale sévère, où l’inflammation déclenche la formation de dépôts fibrineux temporaires. L’aspect lisse et luisant du tissu environnant, ainsi que l’éclat lumineux réfléchi, traduisent une surface encore humide, en pleine réaction inflammatoire. On perçoit bien les détails vasculaires sous-jacents, dilatés et nombreux, signes visibles d’une irritation oculaire intense. L’image, capturée en condition clinique réelle, documente un moment typique de traitement manuel d’une conjonctivite virale avec membranes pseudo-fibrineuses.

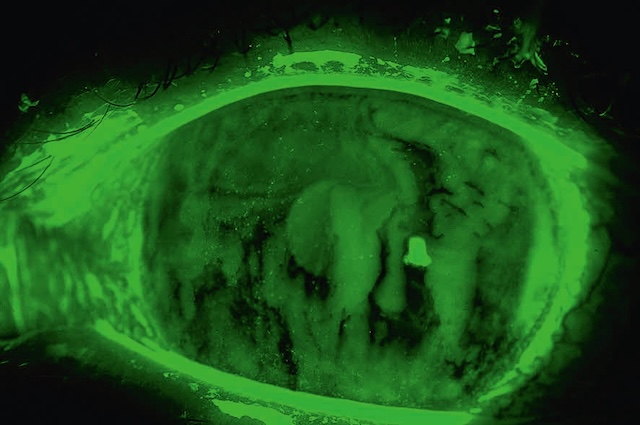
Image en lumière fluorescéine capturée au biomicroscope montrant une kératopathie ponctuée épithéliale due à une sécheresse oculaire sévère. La surface cornéenne présente de multiples zones de coloration ponctuelle, réparties de manière diffuse sur l’épithélium antérieur, traduisant une atteinte du film lacrymal. Les zones d’hyperfluorescence visibles au centre et sur la périphérie de la cornée indiquent une rupture de la barrière épithéliale. Le contour de la cornée est bien délimité et entouré d’une lueur verte uniforme révélée par le colorant, ce qui met en évidence une absence d’humidification homogène. L’image illustre clairement les effets d’un dysfonctionnement de la production lacrymale, typique d’un syndrome sec, avec atteinte inflammatoire chronique de l’œil.

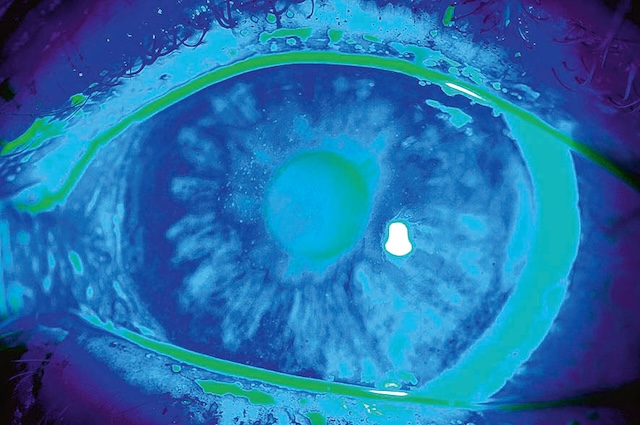
Photographie biomédicale en lumière bleue d’un œil humain réalisée à l’aide de fluorescéine sous lumière ultraviolette, mettant en évidence une kératopathie ponctuée superficielle due à une sécheresse oculaire sévère. Le centre cornéen présente une zone centrale trouble et diffuse, tandis que la périphérie laisse apparaître des lésions ponctiformes réparties radialement, trahissant une rupture du film lacrymal. Les marquages fluorescents révèlent nettement les irrégularités épithéliales, soulignant des microérosions sur l’épithélium cornéen. L’anneau limbique reste relativement préservé, mais l’ensemble suggère une atteinte diffuse en surface cornéenne avec un assèchement marqué du tissu oculaire.


Cette photographie ophtalmologique, réalisée en lumière bleue après instillation de fluorescéine, révèle une kératoconjonctivite sèche localisée à l’espace interpalpébral. L’image est caractérisée par une multitude de points fluorescents répartis en mosaïque dense, visibles sur la surface cornéenne, traduisant des zones de dénudation épithéliale dues à l’altération du film lacrymal. Le tracé bien marqué de l’anneau péricornéen supérieur et inférieur, ainsi que l’absence de coloration homogène centrale, confirment que le défaut de lubrification se concentre dans la zone exposée entre les paupières, typique de la sécheresse oculaire sévère. Ce type de cliché est fondamental pour objectiver l’impact de la xérophtalmie sur la cornée, souvent observée dans les syndromes secs ou les pathologies auto-immunes, et permet de guider le clinicien dans le choix thérapeutique adapté.

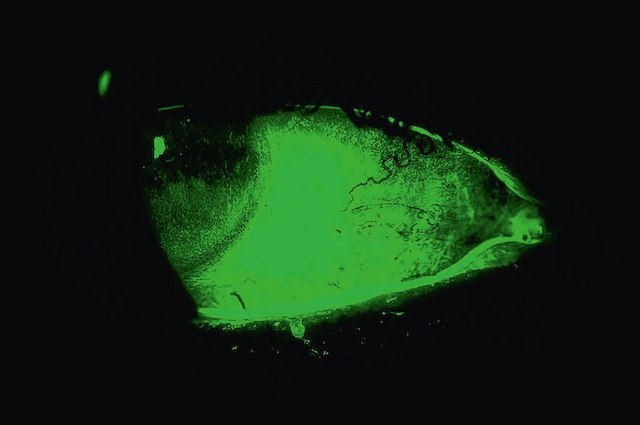
Image clinique obtenue à l’aide de fluorescéine observée sous lumière bleue avec filtre jaune, illustrant de manière nette un marquage épithélial intense au niveau de la zone interpalpébrale, typique d’une kératoconjonctivite sèche modérée à sévère. L’aire centrale de la cornée montre une absorption diffuse du colorant, marquant des altérations étendues de l’épithélium cornéen. On observe également une hyperfluorescence linéaire au niveau de la jonction inférieure, soulignant la stagnation du film lacrymal. La vascularisation conjonctivale périphérique devient visible par transparence, traduisant une irritation oculaire chronique. Ce cliché met en lumière la sévérité de l’atteinte de la surface oculaire, provoquée par une insuffisance de la lubrification naturelle de l’œil.

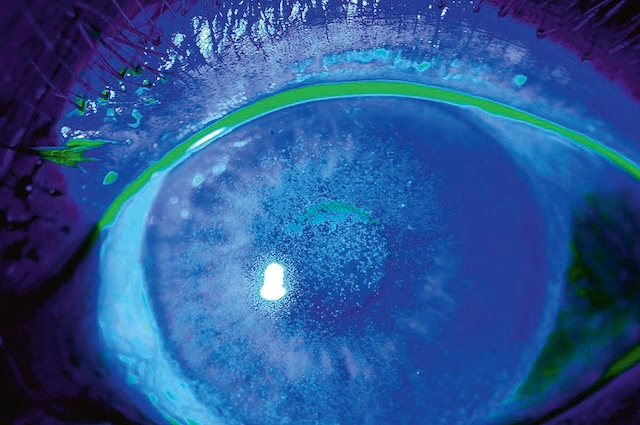
Photographie biomicrographique en lumière bleue cobalt après instillation de fluorescéine montrant une kératoconjonctivite sèche. La zone tarsale supérieure est visible avec quelques cils bien nets et une lueur jaune-vert soulignant le film lacrymal instable au niveau du limbe supérieur. La cornée elle-même révèle une surface relativement régulière mais subtilement marquée par de légères zones de coloration ponctuelle, notamment dans la moitié inférieure, signe d’un dessèchement localisé. L’ensemble de l’image illustre un œil dont la surface oculaire présente une lubrification déficiente, typique du syndrome sec. Le reflet lumineux central accentue la transparence cornéenne, mais masque partiellement les micro-altérations, caractéristiques d’une kératopathie superficielle légère.

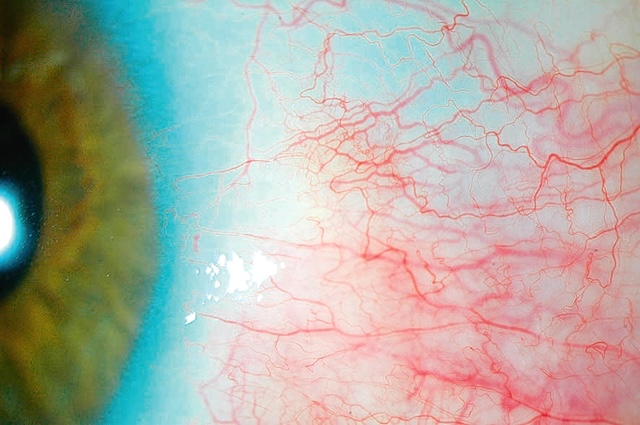
Photographie clinique en lumière naturelle du segment antérieur d’un œil, focalisée sur la sclère temporale, révélant une épisclérite nodulaire localisée. On distingue une zone surélevée légèrement rosée, entourée de vaisseaux épiscléraux dilatés et sinueux, très apparents à la surface, sans atteinte profonde. Le nodule inflammatoire, non douloureux à la palpation dans la majorité des cas, se détache par contraste avec le blanc scléral environnant, encore intact. La périphérie de l’iris brun est visible sur la gauche, tandis que l’intensité de la congestion vasculaire diminue progressivement vers les zones non touchées. L’ensemble suggère une inflammation bénigne mais bien circonscrite de l’épisclère.

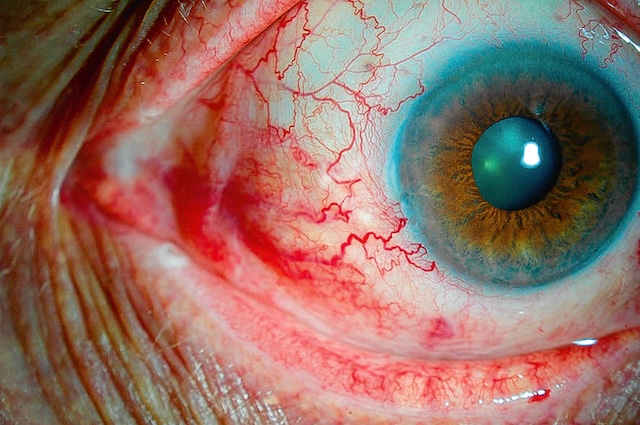
Photographie en très haute résolution d’un œil en lumière naturelle directe, illustrant une épisclérite nasale bien marquée. On observe une injection conjonctivale localisée, avec des vaisseaux dilatés et tortueux concentrés principalement vers la région nasale de l’œil, créant une rougeur intense mais limitée. Ces vaisseaux, superficiels et mobiles à la palpation dans un contexte clinique, sont typiques d’un processus inflammatoire bénin affectant l’épisclère. Le reste de la conjonctive reste relativement épargné, et la cornée, l’iris ainsi que le cristallin apparaissent normaux, avec une transparence maintenue. Cette image restitue fidèlement l’aspect clinique d’une épisclérite simple, souvent idiopathique, généralement indolore, et d’évolution spontanément favorable. Le contraste entre la zone inflammatoire localisée et les structures oculaires adjacentes saines rend cette photo particulièrement illustrative à visée diagnostique.

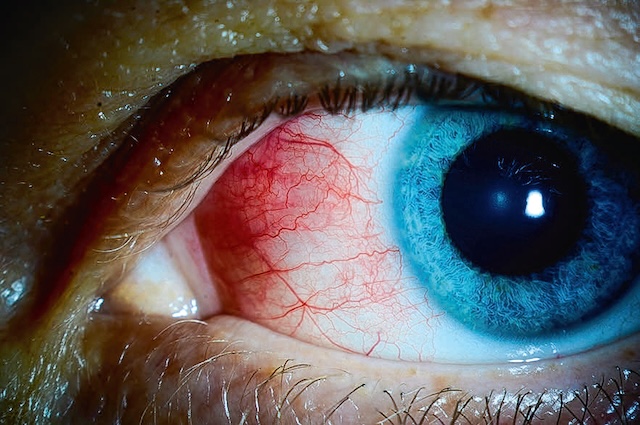
Ce gros plan clinique montre l’œil gauche d’un patient atteint d’une épisclérite nasale, une inflammation localisée et superficielle de l’épisclère. La rougeur bien circonscrite, concentrée du côté nasal, laisse apparaître un réseau de vaisseaux dilatés, fins et sinueux, nettement visibles sous l’éclairage focalisé. Contrairement à une sclérite, la teinte rouge est vive, les vaisseaux restent mobiles à la pression douce, et la douleur rapportée est souvent modérée. L’aspect global de la cornée et de la chambre antérieure est calme, sans signe de réaction inflammatoire profonde. Cette photographie biomédicale est typique d’une observation à la lampe à fente, utile dans le diagnostic différentiel des rougeurs oculaires.
Sclérite nodulaire inférieure droite.

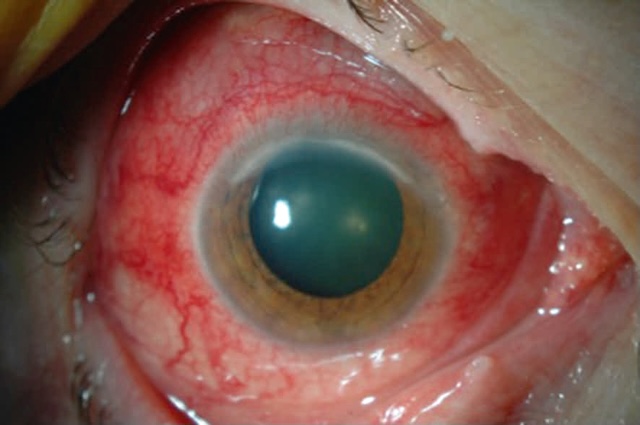
Photographie clinique en lumière naturelle d’un œil droit présentant une sclérite supérieure avec kératite périphérique ulcérante. L’hyperhémie conjonctivale est marquée, surtout au niveau supérieur et temporal, avec des vaisseaux profonds congestionnés suggérant une atteinte sclérale inflammatoire sévère. La cornée montre une opacification en bordure supérieure, traduisant une ulcération périphérique active, accompagnée d’un amincissement localisé et d’un léger floutage stromal adjacent. La zone pupillaire reste claire mais contraste fortement avec l’intensité inflammatoire périphérique. L’aspect global évoque une pathologie auto-immune sous-jacente, possiblement d’origine rhumatologique, avec menace d’atteinte structurelle si non prise en charge rapidement.

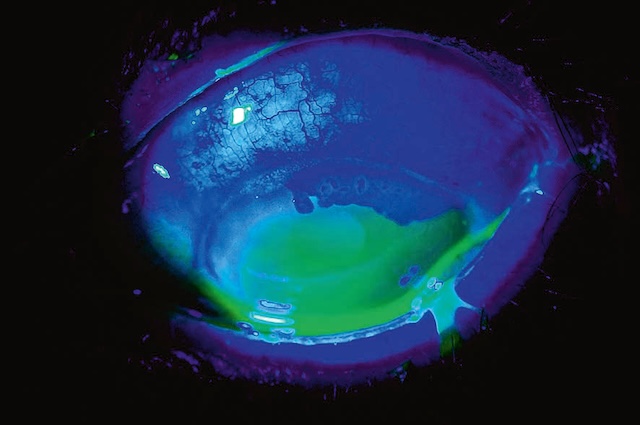
Image d’examen ophtalmologique réalisée sous lumière bleue après instillation de fluorescéine, capturant les effets d’une brûlure chimique sévère sur la surface oculaire. La cornée apparaît largement imprégnée de fluorescéine avec une teinte vert vif au centre, traduisant une ulcération profonde et active. En périphérie, un chémosis conjonctival est visible, avec un soulèvement œdémateux marqué et des vaisseaux engorgés, suggérant une réaction inflammatoire aiguë. La délimitation floue entre les zones saines et lésées met en évidence la gravité du traumatisme chimique. L’image témoigne d’une atteinte étendue de la barrière épithéliale et d’un déséquilibre majeur du film lacrymal consécutif à une agression caustique.

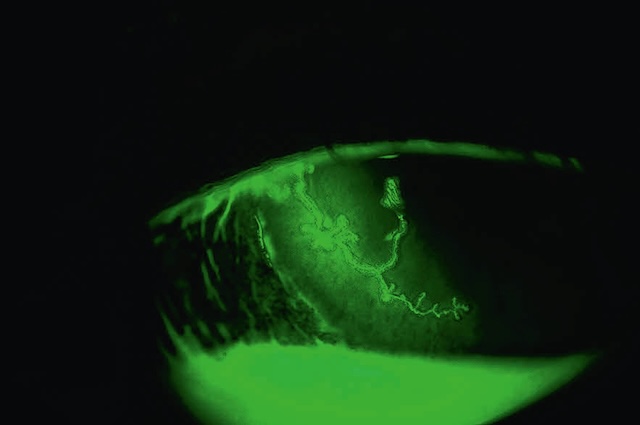
Image biomédicale en lumière ultraviolette après instillation de fluorescéine, révélant avec précision une kératite herpétique dendritique. Sur la surface cornéenne, on observe un tracé finement ramifié, arborant la forme caractéristique d’une lésion dendritique, avec des extrémités bulbeuses bien fluorescentes. Cette lésion serpentine, d’aspect filiforme, est typique d’une infection virale à HSV, affectant l’épithélium cornéen superficiel. Le contraste offert par la fluorescéine met en évidence la structure des atteintes tissulaires, soulignant leur finesse et leur distribution arborescente. L’environnement sombre accentue la clarté des détails lésionnels, donnant une vue directe sur l’activité virale au niveau de la cornée.

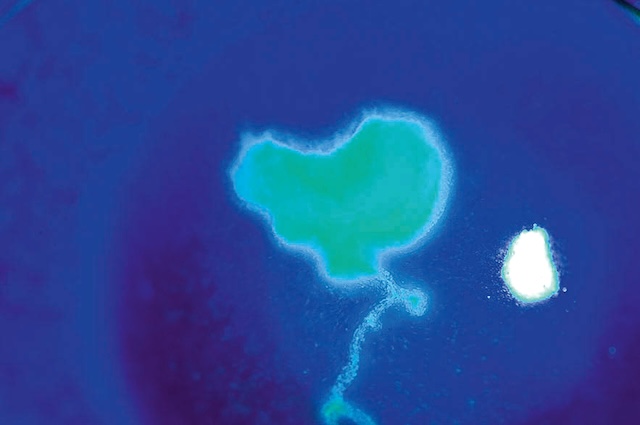
Cette photographie réalisée à la lampe à fente sous lumière bleue après instillation de fluorescéine révèle une ulcération cornéenne particulièrement évocatrice d’une kératite herpétique. On observe une lésion centrale étalée en forme géographique, aux contours irréguliers et flous, soulignée par une coloration verte intense traduisant une perte de l’épithélium cornéen. Prolongeant cette zone, une fine arborisation s’étire vers le bas sous la forme d’un tracé ramifié, typique de la forme dendritique de la kératite à HSV. L’éclairage met en relief l’aspect infectieux actif, avec des bords fluorescents nets contrastant sur le fond cornéen bleu. Ce cliché est un excellent exemple d’une lésion épithéliale virale, exigeant une prise en charge rapide pour éviter une atteinte stromale plus profonde.

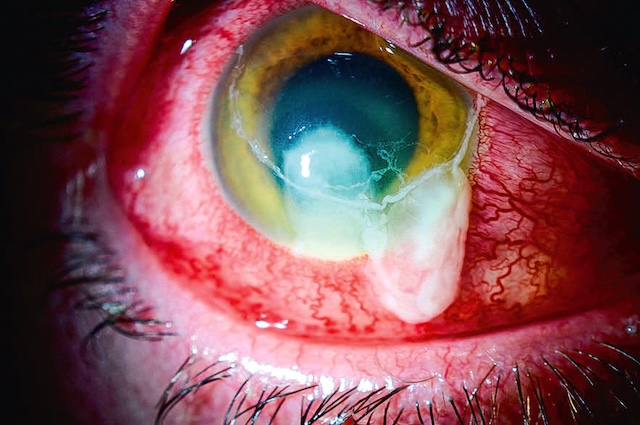
Photographie clinique en lumière blanche montrant un abcès cornéen bactérien sévère accompagné de sécrétions purulentes épaisses. Au centre de la cornée, une infiltration blanchâtre bien délimitée s’étend vers la chambre antérieure, traduisant une infection profonde du stroma cornéen. La surface est surmontée d’un épais dépôt mucopurulent, adhérant à la lésion centrale, signe typique d’un processus infectieux actif. La conjonctive est nettement hyperhémiée, avec une congestion diffuse des vaisseaux superficiels, renforçant l’intensité inflammatoire locale. Le reflet pupillaire est estompé, suggérant une atteinte visuelle significative. Cette image capte avec précision la présentation typique d’un abcès cornéen d’origine bactérienne, associant douleur, baisse d’acuité visuelle et écoulement, nécessitant une prise en charge rapide et intensive. L’ensemble évoque une situation ophtalmologique d’urgence, où l’intégrité de la cornée est clairement menacée.

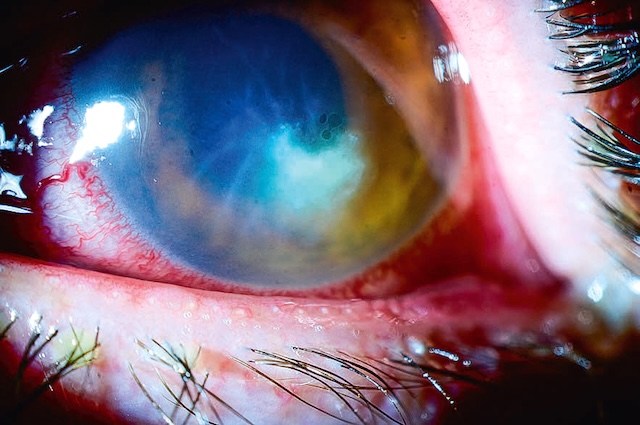
Ce cliché clinique en macrophotographie illustre un cas manifeste d’abcès cornéen fongique, également appelé kératomycose. Au centre de la cornée, une infiltration blanchâtre dense se dessine avec netteté, traduisant la colonisation stromale profonde par des filaments mycéliens. Autour de cette zone, le stroma présente un œdème diffus, avec un aspect légèrement grisâtre, témoin de la réaction inflammatoire intense. La limbe est injectée, marquée par une hyperémie conjonctivale périphérique. Ce type de présentation est typique des infections fongiques, notamment chez les patients porteurs de lentilles ou ayant subi un traumatisme végétal. L’image met en évidence la gravité potentielle de ce tableau, nécessitant une identification rapide du germe et une antifongique spécifique.

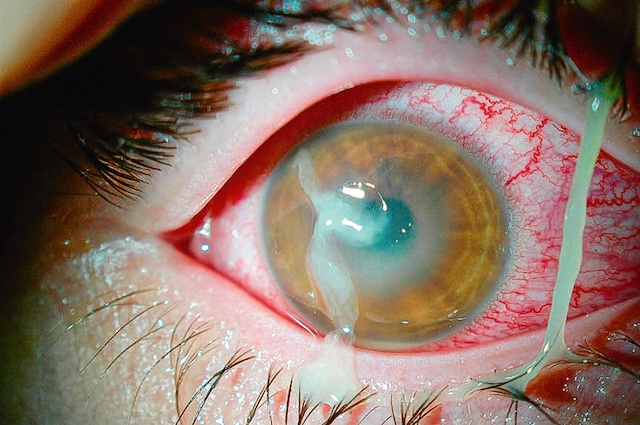
Photographie clinique couleur d’un œil gauche en pleine phase inflammatoire, montrant un abcès cornéen bactérien en cours d’évolution. La cornée présente une opacité blanchâtre dense, localisée au centre, avec des bords flous et infiltrés, signe d’une infection profonde. Une sécrétion purulente abondante, épaisse et filamenteuse s’écoule depuis le cul-de-sac conjonctival inférieur, trahissant une réponse inflammatoire aiguë. L’hyperhémie conjonctivale est marquée, avec une injection diffuse des vaisseaux superficiels. L’aspect luisant du film lacrymal, les cils humides et les traces de pus renforcent le caractère infectieux sévère de cette présentation. Cette image capture un tableau typique d’abcès cornéen nécessitant une intervention rapide.

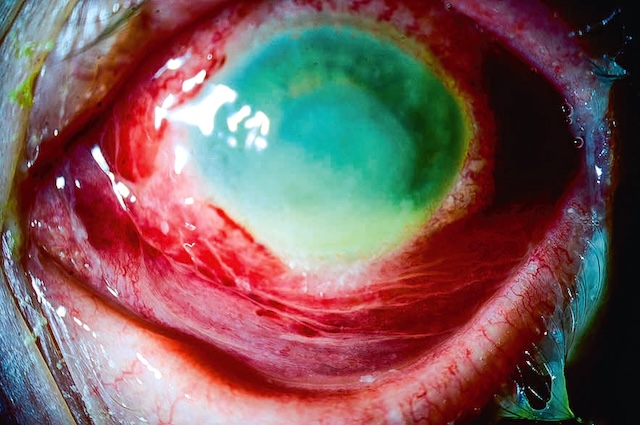
Photographie en haute résolution d’un œil gauche présentant un abcès cornéen bactérien en phase aiguë, avec présence manifeste de sécrétions purulentes. La cornée centrale est envahie par une large zone blanchâtre d’aspect dense, opaque, avec des bords irréguliers mal définis, traduisant une nécrose tissulaire profonde. L’infiltrat occupe le stroma moyen à profond, provoquant un effet de flou visuel intense. La conjonctive est intensément congestive, injectée en nappe, avec une chemosis notable et un larmoiement abondant. Une accumulation de sécrétions blanchâtres et épaisses est visible à la jonction palpébrale inférieure, signe de l’infection bactérienne active. L’ensemble témoigne d’une kératite suppurée sévère, nécessitant une antibiothérapie d’urgence pour éviter la perforation.

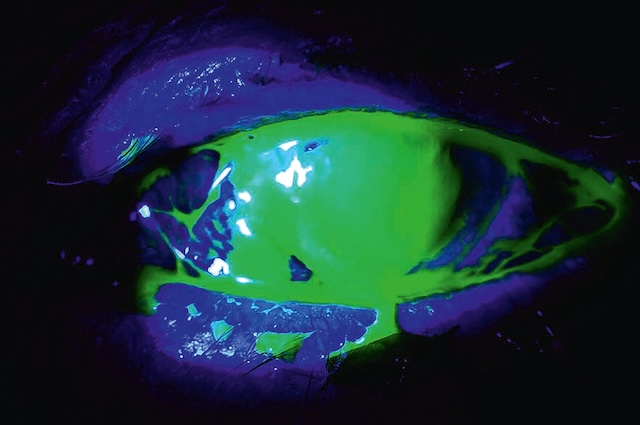
Image biomédicale obtenue sous lumière bleue après instillation de fluorescéine, mettant en évidence un abcès cornéen d’origine bactérienne accompagné de sécrétions abondantes. La cornée apparaît massivement colorée en vert vif, signe d’une altération sévère de l’épithélium, tandis que l’abcès, non clairement délimité ici, se confond dans l’intensité du marquage. De larges traînées de fluorescéine imprègnent les sécrétions mucopurulentes, visiblement accumulées au niveau des paupières et sur toute la surface oculaire. Les reflets brillants traduisent la présence de pus et d’un film lacrymal perturbé. Ce tableau témoigne d’une infection cornéenne active, avec atteinte de la surface oculaire et production inflammatoire importante.

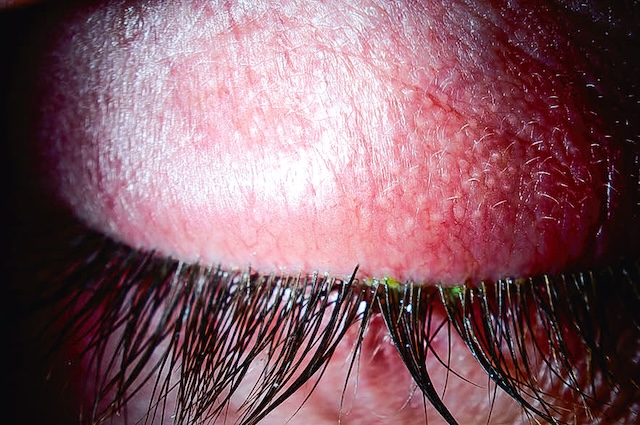
Photographie en lumière directe centrée sur la paupière supérieure, illustrant un œdème palpébral associé à un abcès cornéen sous-jacent. La peau de la paupière apparaît tendue, luisante, et rosée, témoignant d’un gonflement inflammatoire important. Les plis cutanés sont atténués et la texture cutanée est légèrement épaissie, avec un discret érythème diffus. À la racine des cils, on perçoit quelques dépôts séreux ou purulents, signe d’un écoulement lié à l’infection cornéenne. Les cils restent alignés, mais le bord palpébral semble légèrement infiltré. Cet aspect traduit la propagation de l’inflammation depuis la cornée vers les tissus périoculaires, provoquant un œdème réactionnel de la paupière. L’image restitue avec justesse l’un des signes cliniques fréquents d’un abcès cornéen avancé, où les tissus palpébraux deviennent douloureusement engorgés.

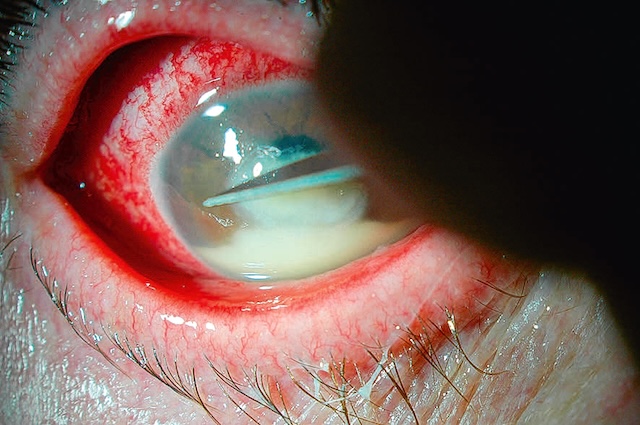
Photographie clinique en lumière focalisée montrant un prélèvement en cours sur un abcès cornéen à l’aide d’une lame stérile fine. L’œil, visiblement très inflammé, présente une hyperhémie conjonctivale marquée et une opacité dense de la cornée inférieure, de couleur blanchâtre, correspondant à l’infiltrat purulent. La lame, introduite avec précision sur la zone infectée, est en contact direct avec le centre de l’abcès afin de recueillir le matériel pour analyse microbiologique. Une couche dense d’exsudat purulent tapisse le segment antérieur, témoin d’un processus infectieux sévère. Ce cliché illustre un moment clé du diagnostic étiologique d’une kératite infectieuse, capturé en pleine procédure.

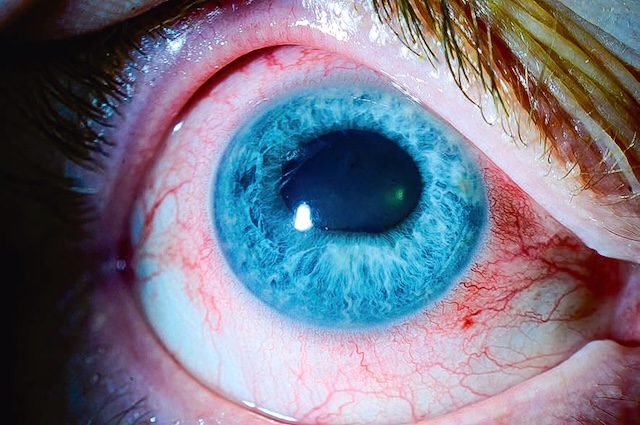
Photographie clinique prise en éclairage focalisé, montrant un œil atteint d’une uvéite antérieure avec injection ciliaire bien marquée. Les vaisseaux autour de la limbe sont dilatés, formant une couronne rouge violacée caractéristique d’une inflammation intraoculaire. La pupille présente une déformation notable, secondaire à des synéchies postérieures, où l’iris adhère à la capsule du cristallin. La chambre antérieure paraît légèrement trouble, suggérant une réaction inflammatoire active. L’iris, aux cryptes bien visibles, se retrouve tiré vers certaines zones, modifiant la régularité du bord pupillaire. Cette image illustre parfaitement une réponse inflammatoire intense localisée à l’uvée antérieure avec complication pupillaire.

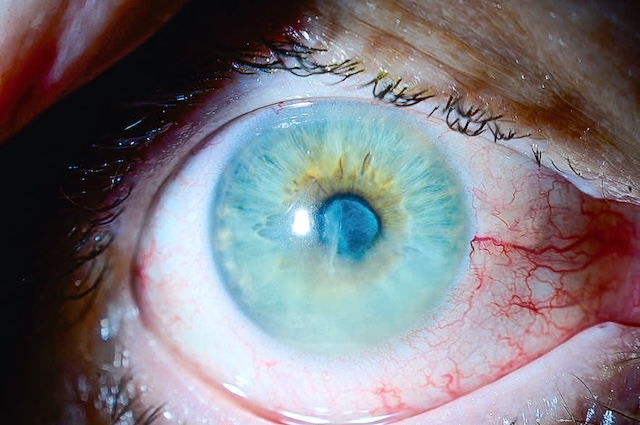
Photographie clinique en lumière dirigée, capturant un œil atteint d’une uvéite antérieure aiguë avec des signes très caractéristiques. La cornée apparaît discrètement œdémateuse, et une opacité grisâtre est visible au niveau de la chambre antérieure, correspondant à un hypopion sédimenté. Juste en arrière de la cornée, une membrane cyclitique blanchâtre, fine mais bien formée, se dessine en semi-cercle, traduisant une réponse inflammatoire marquée de l’uvée. L’iris, aux reliefs flous, semble partiellement englué, et la pupille n’a plus sa forme régulière. On note également une injection conjonctivale diffuse et marquée. Cette image illustre un épisode inflammatoire intraoculaire intense, nécessitant une prise en charge urgente.
